ОТ ГЛАВНОГО РЕДАКТОРА
КЛИНИЧЕСКАЯ ФАРМАКОГЕНЕТИКА
Что уже известно об этой теме?
Ключевая роль статинов: аторвастатин и другие статины являются основой терапии ишемической болезни сердца (ИБС) для снижения уровня «плохого» холестерина (ХС-ЛПНП) и риска сердечно-сосудистых осложнений.
Различный ответ на терапию: не все пациенты достигают целевых уровней холестерина. Причины могут включать генетические особенности, приверженность лечению, диету и сопутствующие препараты.
Влияние генетики (CYP3A4): аторвастатин метаболизируется в печени ферментом CYP3A4. Генетические полиморфизмы (вариации) в гене CYP3A4 могут изменять активность этого фермента, влияя на концентрацию препарата в крови и его эффективность.
Противоречивые данные: результаты предыдущих исследований о влиянии конкретного полиморфизма rs2740574 (A/G) противоречивы. Одни работы связывают вариант G со сниженной активностью фермента (более сильный эффект), другие — с повышенной активностью (ослабленный эффект).
Что нового даёт статья?
Уникальные популяционные данные: впервые изучена частота трёх полиморфизмов гена CYP3A4 у пациентов с ИБС в Архангельске (северный регион России). Обнаружено, что частота «мутантного» аллеля G (rs2740574) составляет 8,3%, что значимо выше, чем в общероссийской (4%) и европейской (3,63%) популяциях.
Связь с лучшим ответом: исследование показало, что носители аллеля G (rs2740574) в этой популяции имеют достоверно более выраженное снижение общего холестерина и ХС-ЛПНП через 2–4 месяца терапии аторвастатином по сравнению с носителями распространённого аллеля A.
Редкость других вариантов: подтверждено, что два других изученных полиморфизма (Leu293Pro и Phe189Ser) встречаются крайне редко (0–0,5%) в данной выборке, поэтому их влияние на эффективность терапии у большинства пациентов будет незначимым.
Как это может повлиять на клиническую практику в обозримом будущем?
Персонализация терапии: результаты поддерживают потенциал использования фармакогенетического тестирования перед назначением статинов. Выявление аллеля G может помочь врачу предсказать, что пациент будет хорошо отвечать на терапию аторвастатином.
Оптимизация выбора препарата и дозы: знание генотипа могло бы помочь в выборе стартовой дозы аторвастатина или в обосновании выбора именно этого препарата для достижения целевых уровней липидов.
Необходимость подтверждения: авторы подчёркивают, что из-за небольшого размера выборки результаты являются предварительными. Для внедрения тестирования в рутинную практику необходимы более масштабные многоцентровые исследования, которые подтвердят надёжность этого генетического маркера для прогнозирования эффективности лечения.
Актуальность. Одним из ведущих направлений персонализированной медицины является фармакогенетика, позволяющая спрогнозировать эффективность и безопасность применения лекарственных средств у конкретного пациента. В исследовании проанализировано наличие мутации аллелей гена CYP3A4 и их связь с эффективностью терапии.
Цель исследования. Оценить влияние генетического полиморфизма A/G (rs2740574) гена CYP3A4, а также полиморфизмов CYP3A4_2 Leu293Pro (rs28371759) и CYP3A4 Phe189Ser (rs4987161) у пациентов с ишемической болезнью сердца (ИБС) на гиполипидемическую эффективность аторвастатина в реальной клинической практике.
Материалы и методы. В исследование включено 96 пациентов с ИБС, получавших терапию аторвастатином. Методом полимеразной цепной реакции в реальном времени проведён молекулярно-генетический анализ полиморфизмов гена CYP3A4. Статистическая обработка данных выполнена с использованием программы «STATA 14».
Результаты. В исследуемой выборке частота аллеля G (rs2740574) составила 8,3 %, что значимо отличается от общероссийской (4 %, p = 0,0095) и европейской (3,63 %, p = 0,0005) популяций. Для полиморфизма CYP3A4_2 Leu293Pro (rs28371759) частота минорного аллеля C составила 0,5 %, что также значимо отличается от мировых и европейских частот (p < 0,001). Полиморфизм CYP3A4 Phe189Ser (rs4987161) в выборке обнаружен не был. У носителей аллеля G (rs2740574) (n = 15) на фоне терапии аторвастатином зафиксировано достоверное снижение уровня общего холестерина (с 5,38 ± 1,49 до 3,23 ± 0,96 ммоль/л, p = 0,0019) и ХС-ЛПНП (с 3,54 ± 1,17 до 1,58 ± 0,62 ммоль/л, p = 0,0004). Влияние других полиморфизмов на липидный профиль оценить не удалось ввиду их низкой распространённости.
Заключение. У пациентов с ИБС в г. Архангельске выявлены уникальные частоты аллелей генов CYP3A4, отличающиеся от референсных популяций. Наличие аллеля G (rs2740574) ассоциировано с более выраженным гиполипидемическим ответом на терапию аторвастатином. Полученные данные подчёркивают важность фармакогенетических исследований для персонализации терапии статинами.
Что уже известно об этой теме?
Роль GST: гены глутатион-S-трансфераз (GSTM1 и GSTT1) кодируют ферменты детоксикации ксенобиотиков, включая химиотерапевтические препараты (циклофосфамид, доксорубицин, таксаны), используемые при раке молочной железы (РМЖ).
Полиморфизм: наиболее изученными являются «нулевые» (делеционные) варианты этих генов, приводящие к отсутствию ферментативной активности.
Противоречия в данных: ранее опубликованные данные были неоднозначны:
Одни исследования показывали, что «нулевые» генотипы повышают эффективность химиотерапии (лучший ответ, снижение риска рецидива) за счет замедленного выведения цитостатиков.
Другие работы (включая мета-анализы) не находили значимой связи между этими полиморфизмами и выживаемостью пациентов.
Исследования в основном проводились без углубленной стратификации по биологическим подтипам опухоли и стадиям заболевания.
Что нового даёт статья?
Стратификация по клиническим признакам: впервые на российской популяции (Приморский край) проведен детальный анализ эффективности химиотерапии в зависимости от делеционного статуса GSTT1 и GSTM1 с разделением пациентов не только по возрасту, но и по стадии и молекулярно-биологическим подтипам РМЖ.
Конкретные ассоциации:
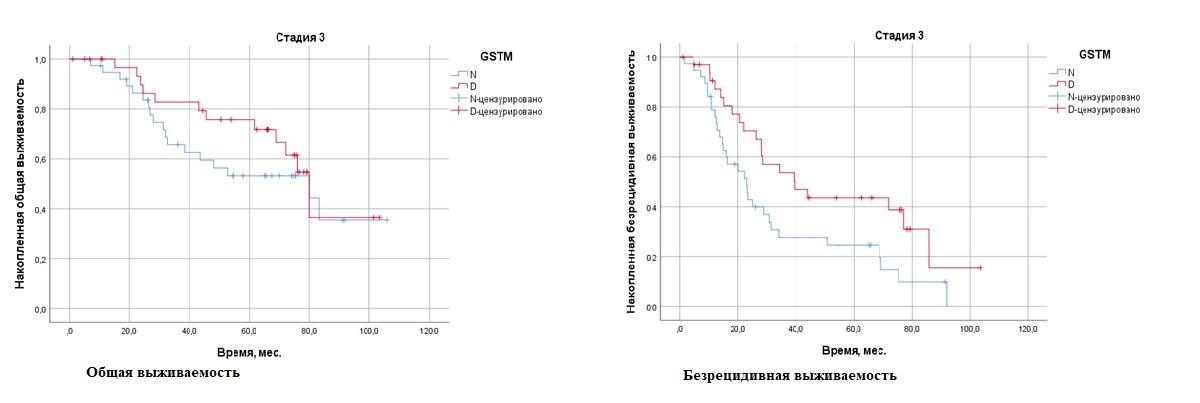
III стадия: наличие «нулевых» генотипов GSTM1 и GSTT1 статистически значимо повышает безрецидивную выживаемость у пациентов с III стадией заболевания. Риск рецидива снижался в 0,52 и 0,4 раза соответственно.
Гормонозависимые подтипы:
При люминальном A и люминальном B HER2-негативном подтипах наличие делеции GSTT1 ассоциировалось с отсутствием летальных исходов (значимое повышение общей выживаемости).
При люминальном B HER2-негативном подтипе делеция GSTM1 также значимо снижала риск рецидива.
При люминальном B HER2-позитивном подтипе у пациенток с делецией GSTM1 не было зарегистрировано летальных исходов.
Возраст: статистически значимого влияния возраста манифестации заболевания на связь между полиморфизмом и выживаемостью не выявлено.
Как это может повлиять на клиническую практику в обозримом будущем?
Уточнение прогноза: фармакогенетическое тестирование на «нулевые» генотипы *GSTT1/GSTM1* может стать дополнительным инструментом для прогнозирования эффективности химиотерапии, особенно у пациентов с местнораспространенным (III стадия) и гормонозависимым (люминальные подтипы) РМЖ.
Персонализация терапии: врачи смогут учитывать генетический статус пациента при выборе тактики лечения:
Пациентам с «нулевыми» генотипами (которые выводят препараты медленнее) стандартная химиотерапия может давать лучший противоопухолевый эффект, что позволяет увереннее назначать интенсивные схемы.
Это знание может помочь избежать необоснованной эскалации терапии или, наоборот, оправдать её применение у пациентов с высоким риском рецидива (III стадия), если у них обнаружен благоприятный для ответа генотип.
Экономическая целесообразность: обоснованное назначение дорогостоящих препаратов или интенсивных режимов на основе генетического теста (с учетом доказанного преимущества для конкретной подгруппы) может повысить эффективность затрат в здравоохранении.
Ограничение: авторы сами отмечают, что выборка по некоторым подтипам небольшая, что требует подтверждения на более масштабных группах, прежде чем внедрять эти маркеры в рутинные клинические рекомендации.
Актуальность. Неуклонный рост заболеваемости раком молочной железы (РМЖ), а также связанной с ним смертности и инвалидизации населения обуславливает актуальность поиска эффективного лечения и профилактики данной патологии.
Цель. Оценка различий эффективности химиотерапии РМЖ в зависимости от возраста, стадии и биологического подтипа опухоли с учётом деле- ционного статуса генотипов GSTT1, GSTM1 у пациенток.
Материалы и методы. Проанализированы данные 132 пациенток с РМЖ, получавших химиотерапевтическое лечение в период с 2013 по 2021 гг. Генотипирование полиморфных вариантов GSTM1 и GSTT1 проводили с помощью мультиплексной полимеразной цепной реакции с последующим анализом кривых плавления продуктов реакции.
Результаты. Наличие «нулевого» генотипа GSTМ1 и GSTT1 снижало риск развития рецидива у пациентов с III стадией заболевания в 0,52 раза (95 % ДИ 0,29–0,89, р = 0,023) и 0,4 раза соответственно (95 % ДИ 0,098–0,99, р = 0,049). Среди пациентов с люминальным В HER2-позитивным РМЖ и GSTM1-0 летальных случаев не было, у женщин с люминальным В HER2-негативным подтипом РМЖ риск рецидива снижался в группе с генотипом GSTМ1-0. У пациенток с люминальным A общая выживаемость (ОВ) при «диком» типе GSTT1 составила 75,5 (±12,3) %, при GSTМ1-0-летальных исходов не было (ОР = 0,034, 95 % ДИ 0,02–0,045, р = 0,001), при люминальном B HER2-негативном подтипе ОВ при «диком» типе GSTT1 — 69,9 (±8,5) % против отсутствия летальных случаев при «нулевом» генотипе (ОР = 0,035, 95 % ДИ 0,025–0,044, р = 0,001)).
Заключение. Результаты нашего исследования показали значимое влияние делеционного полиморфизма генов GSTT1 и GSTM1 на безрецидивную выживаемость у пациентов с III стадией заболевания и гормонозависимым раком молочной железы.
Что уже известно об этой теме?
Вариабельность ответа на морфин: фармакокинетика и анальгетический эффект морфина характеризуются высокой межиндивидуальной вариабельностью, что затрудняет подбор безопасной и эффективной дозы.
Роль гена ABCB1: ген ABCB1 (MDR1) кодирует белок-транспортер P-гликопротеин (P-gp), который ограничивает проникновение морфина через гематоэнцефалический барьер и влияет на его всасывание и выведение.
Влияние полиморфизмов: определенные однонуклеотидные полиморфизмы (SNP) в гене ABCB1 (rs1128503, rs2032582, rs1045642) могут изменять экспрессию или функцию P-gp.
Зарубежные данные: исследования на других популяциях (например, итальянской) показали связь между этими полиморфизмами, особенно rs1045642 (C3435T), и эффективностью обезболивания морфином, а также риском развития побочных эффектов.
Что нового даёт статья?
Данные по российской когорте: впервые на российской популяции пациентов паллиативного профиля (86 человек) подтверждена связь между тремя полиморфизмами ABCB1 и концентрацией морфина в плазме крови (а не только с клиническим эффектом).
Количественная оценка: показано, что носительство минорных аллелей (особенно гомозиготного ТТ-генотипа по rs1045642 и rs2032582) ассоциировано со статистически значимо более высокой равновесной концентрацией морфина в плазме.
Пример: для rs1045642 в группе дозы 80–100 мг/сут медиана концентрации у ТТ составила 151,8 нмоль/л против 83,7 нмоль/л у СС.
Дозозависимый эффект: выявлено, что генотип-специфические различия в концентрации становятся наиболее выраженными и достигают статистической значимости в группах пациентов, получающих средние и высокие дозы морфина (40–60 мг и 80–100 мг/сут).
Как это может повлиять на клиническую практику в обозримом будущем?
Персонализация начальной дозы: предварительное генотипирование по ABCB1 может помочь стратифицировать пациентов на группы риска.
Носители ТТ-генотипа (rs1045642, rs2032582): требуют более низких стартовых доз и тщательного мониторинга из-за риска кумуляции (накопления) препарата и передозировки.
Носители СС-генотипа («дикий тип»): могут демонстрировать относительную резистентность к терапии, что потребует более быстрой титрации дозы или рассмотрения альтернативных опиоидов.
Повышение безопасности терапии: учет генетических предикторов позволит снизить частоту нежелательных явлений (сонливость, угнетение дыхания, токсические эффекты), связанных с высокой концентрацией морфина у генетически предрасположенных пациентов.
Интеграция тестирования в алгоритмы: результаты обосновывают целесообразность включения фармакогенетического тестирования по гену ABCB1 в клинические рекомендации и алгоритмы ведения боли в паллиативной онкологии для оптимизации соотношения «эффективность/безопасность».
Актуальность. Фармакокинетика морфина у онкологических пациентов характеризуется высокой межиндивидуальной вариабельностью, отчасти обусловленной генетическими факторами. До настоящего времени роль полиморфизмов гена ABCB1 в модификации экспозиции морфина у данной категории пациентов изучена недостаточно.
Цель. Оценить влияние полиморфизмов rs1128503, rs2032582 и rs1045642 гена ABCB1 на равновесную концентрацию морфина в плазме крови у пациентов с онкологическими заболеваниями, получающих терапию в условиях паллиативной помощи.
Методы. В исследование включены 86 онкологических пациентов, находившихся на лечении в паллиативном отделении ГБУЗ «Московский много- профильный центр паллиативной помощи» Департамента здравоохранения города Москвы. Все участники получали морфин перорально в стабильных дозах от 30 до 100 мг/сут. Генотипирование полиморфизмов ABCB1 проводилось методом ПЦР в режиме реального времени. Концентрации морфина в плазме определялись методом ВЭЖХ-МС/МС. Статистический анализ включал оценку нормальности распределения (критерий Шапиро–Уилка), непараметрические критерии Манна–Уитни и Краскела–Уоллиса, χ², p ≤ 0,05 считалось статистически значимым.
Результаты. У носителей ТТ-генотипа rs1045642 при дозе 80–100 мг/сут медианная концентрация морфина составила 151,8 нмоль/л, превышая значения у CT (110,4 нмоль/л) и CC (83,7 нмоль/л), при p = 0,097 (χ²), p ≤ 0,05 для парных сравнений. Аналогичные тенденции выявлены для rs2032582 и rs1128503, с достоверными различиями между носителями минорных аллелей. Нежелательных явлений, связанных с исследуемым вмешательством, не зарегистрировано.
Заключение. Носительство определённых аллельных вариантов ABCB1 ассоциировано с повышенной экспозицией морфина. Учёт генетических предикторов может способствовать индивидуализации дозирования у онкологических пациентов, получающих паллиативную терапию.
Что уже известно об этой теме?
Высокий риск ВТЭО: после тотального эндопротезирования коленного сустава (ТАКС) существует высокий риск венозных тромбоэмболических осложнений (ВТЭО), что требует обязательной профилактики антикоагулянтами.
Применение ПОАК: прямые оральные антикоагулянты (ПОАК), включая дабигатран, эффективны и удобны для профилактики ВТЭО, но их эффективность и безопасность имеют значительную межиндивидуальную вариабельность.
Влияние генов: известно, что на фармакокинетику дабигатрана могут влиять полиморфизмы генов, отвечающих за транспорт (гликопротеин-Р, ген ABCB1) и метаболизм (карбоксилэстераза, ген CES1) препарата.
Что нового даёт статья?
Конкретные ассоциации «генотип-исход»: исследование наглядно демонстрирует клинические последствия носительства определенных генотипов:
ABCB1 (3435TT): ассоциирован с повышенной концентрацией дабигатрана и высоким риском кровотечений (случаи №1, №5).
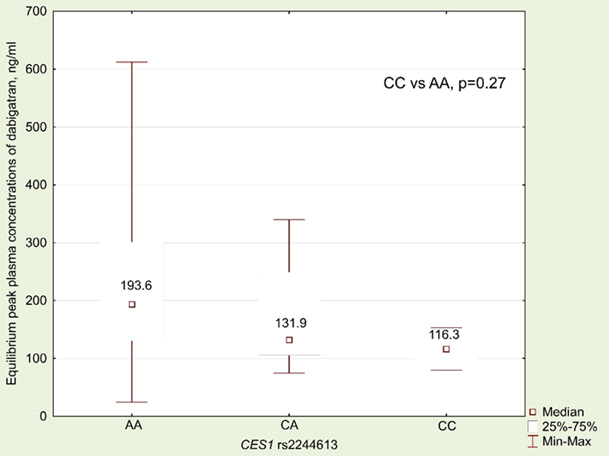
CES1 (rs2244613 CC): коррелирует с более низкой концентрацией препарата и, как следствие, повышенным тромботическим риском (случай №1).
«Непредсказуемый» генотип: впервые акцентируется внимание на том, что гетерозиготное носительство по всем трем изученным полиморфизмам дает наиболее непредсказуемый эффект в плане развития как тромбозов, так и кровотечений (случай №4).
Выявление «благоприятного» генотипа: описан вариант комбинации генотипов (ABCB1 CC + ABCB1 ТТ + CES1 AA), который, несмотря на высокий исходный риск тромбозов, обеспечил высокую эффективность и безопасность терапии (случай №3).
Роль лекарственных взаимодействий: подробно разобран случай тяжелого кровотечения, вызванного не только генетикой, но и фармакокинетическим/динамическим взаимодействием дабигатрана с часто назначаемыми препаратами (амлодипин, лизиноприл, розувастатин, фондапаринукс) (случай №6).
Потенциал теста тромбодинамики: показано, что тест тромбодинамики может быть перспективным инструментом для диагностики гиперкоагуляции и мониторинга эффективности терапии дабигатраном на индивидуальном уровне.
Как это может повлиять на клиническую практику в обозримом будущем?
Персонализация выбора дозы: знание генотипов ABCB1 и CES1 до начала лечения позволит выделить пациентов с высоким риском кровотечений (для рассмотрения вопроса о снижении дозы) и пациентов с риском неэффективности терапии (для рассмотрения вопроса об увеличении дозы или смене препарата).
Предиктивное тестирование: внедрение предварительного генетического тестирования может стать рутинным этапом перед назначением дабигатрана для профилактики ВТЭО в ортопедии, чтобы заранее предсказать индивидуальный ответ на терапию.
Учет лекарственных взаимодействий: статья подчеркивает необходимость тщательной оценки сопутствующей терапии (статины, блокаторы кальциевых каналов и др.) для предотвращения опасных лекарственных взаимодействий, особенно у генетически предрасположенных пациентов.
Комплексный подход: предложена модель персонализированного подхода, сочетающего генетическое тестирование, терапевтический лекарственный мониторинг (определение концентрации) и функциональные тесты (тромбодинамика) для максимальной безопасности и эффективности антикоагулянтной терапии.
Введение. Эффективность и безопасность дабигатрана для профилактики венозных тромбоэмболических осложнений (ВТЭО) характеризуются значительной межиндивидуальной вариабельностью, которая частично обусловлена фармакогенетическими факторами.
Цель. Оценить влияние полиморфизмов генов ABCB1 (rs1045642, rs4148738) и CES1 (rs2244613) на фармакокинетику дабигатрана и клинические исходы у пациентов после ортопедических операций.
Методы. В исследование были включены 60 пациентов, получавших дабигатрана этексилат (220 мг/сут) после тотального эндопротезирования коленного сустава. Генотипирование проводили методом ПЦР в реальном времени, концентрацию дабигатрана в плазме определяли методом ВЭЖХ-МС/МС. Оценивали клинические исходы (ВТЭО, кровотечения).
Результаты. Генотип ABCB1 3435TT был ассоциирован с более высокой концентрацией дабигатрана и повышенным риском кровотечений, в то время как генотип CES1 rs2244613 CC коррелировал с более низкой концентрацией и повышенным тромботическим риском. Комбинация генотипов ABCB1 (CC и TT) и CES1 (AA) продемонстрировала оптимальную эффективность и безопасность. Гетерозиготное носительство всех трёх полиморфизмов имело непредсказуемый эффект. Описан случай тяжелого кровотечения, связанного с лекарственным взаимодействием.
Вывод. Полиморфизмы генов ABCB1 и CES1 значимо влияют на экспозицию дабигатрана и риск осложнений. Предиктивное генетическое тести- рование может способствовать персонализации антикоагулянтной терапии для повышения её безопасности и эффективности у послеоперационных пациентов.
ЭТНИЧЕСКИЕ АСПЕКТЫ ФАРМАКОГЕНЕТИКИ
Что уже известно об этой теме?
Роль ферментов: бедаквилин (ключевой препарат для лечения лекарственно-устойчивого туберкулеза) метаболизируется в печени изоферментом CYP3A4 цитохрома Р450.
Влияние генетики: полиморфизмы (генетические вариации) в генах CYP3A4 и CYP3A5 могут приводить к изменению активности этих ферментов, что влияет на концентрацию препарата в крови, а значит — на эффективность лечения и риск побочных эффектов.
Популяционные различия: распространенность этих полиморфизмов существенно различается между разными этническими группами (например, у европейцев и азиатов). В частности, вариант CYP3A4*22 редок у азиатов, но встречается у европейцев, а CYP3A5*3 распространен повсеместно, но с разной частотой.
Пробел в знаниях: до этого исследования отсутствовали данные о частоте встречаемости ключевых полиморфизмов (CYP3A4*22 и CYP3A5*3) среди коренного населения Якутии (якутов) и русских, проживающих в этом регионе и больных туберкулезом.
Что нового даёт статья?
Уникальные данные по якутам: впервые получены данные о распределении генотипов CYP3A4*22 и CYP3A5*3 среди якутов, больных лекарственно-устойчивым туберкулезом. Выявлено, что якуты статистически значимо отличаются по этим показателям от восточных азиатов (китайцев, японцев и др.), несмотря на географическую близость.
Особенности русских в Якутии: русские, проживающие в Якутии, по профилю CYP3A5*3 не отличаются от общеевропейской популяции. Однако по гену CYP3A4*22 они продемонстрировали почти полное отсутствие «медленного» аллеля (T), что отличает их от европейцев, но сближает с азиатскими популяциями.
Объединенная "сибирская" характеристика: при сравнении объединенной группы "сибиряков" (якуты + русские Якутии) с общей евразийской выборкой (европейцы + восточные азиаты) выявлено, что у сибиряков:
Значительно реже встречается «медленный» аллель гена CYP3A4*22.
Значительно чаще встречается «медленный» гомозиготный генотип GG по гену CYP3A5*3.
Фенотипы метаболизма: показано, что подавляющее большинство как якутских, так и русских пациентов являются промежуточными метаболизаторами лекарств через CYP3A. Фенотип медленного метаболизма встречается крайне редко (только у 1% якутов).
Как это может повлиять на клиническую практику в обозримом будущем?
Персонализация терапии бедаквилином: высокая частота «медленного» генотипа CYP3A5*3 (GG) в сибирской популяции означает, что у этих пациентов может быть снижена скорость выведения бедаквилина. Это потенциально может приводить к более высоким концентрациям препарата в крови.
Прогнозирование рисков: знание своего генотипа может помочь врачам заранее выявлять пациентов с риском более высокой концентрации бедаквилина (и, следовательно, повышенным риском побочных эффектов, таких как удлинение интервала QT на ЭКГ), а также пациентов с риск развития неэффективности лечения.
Обоснование для тестирования: выявленные межпопуляционные различия подчеркивают необходимость более широкого внедрения фармакогенетического тестирования перед назначением бедаквилина в регионах с смешанным и уникальным генофондом (как в Якутии). Это позволит перейти от стандартных доз к индивидуальному подбору терапии для повышения ее эффективности и безопасности.
Обоснование. Лечение лекарственно-устойчивого туберкулёза сопряжено с множеством медико-социальных проблем, поэтому продолжается поиск мер по улучшению результатов лечения с помощью разработки новых лекарств и схем химиотерапии. Бедаквилин метаболизируется изоферментом цитохрома P450 CYP3A4. Полиморфизмы CYP3A4 и CYP3A5 могут приводить к вариабельности концентраций бедаквилина в плазме, и влиять на эффективность и безопасность лечения. В настоящее время отсутствуют данные о распространённости полиморфных вариантов гена CYP3A4*22 и CYP3A5*3 среди якутов и русских, больных туберкулёзом.
Цель. Изучить частоту носительства полиморфизмов генов CYP3A4*22 (rs35599367) C>T, CYP3A5*3 (rs776746) A>G среди якутов и русских, больных лекарственно-устойчивым туберкулёзом в сравнении с нормальной изменчивостью аллельных вариантов изучаемых генов в восточноазиатских и европейских популяциях.
Методы. Определяли полиморфизмы CYP3A4*22 (rs35599367) C>T, CYP3A5*3 (rs776746) A>G методом полимеразной цепной реакции в режиме реального времени.
Результаты. Частота аллеля T гена CYP3A4*22 достоверно ниже в сибирской группе по сравнению с частотой в евразийской группе (p = 0,003). Генотип дикого типа (CC) CYP3A4*22 встречался значимо чаще в сибирской группе больных, чем в евразийской группе, гетерозиготный генотип (CT) меньше представлен в сибирской популяции (p = 0,003). Генотип AA CYP3A5*3 реже встречался в сибирской группе пациентов относительно его частоты в евразийской группе (p = 0,021), гетерозиготный генотип AG намного реже выявлялся в сибирской популяции больных (p < 0,001), генотип GG преобладал в сибирской группе и реже определялся в евразийской популяции (p < 0,001). Выявлены различия распределение аллелей и генотипов CYP3A5*3 между якутами и восточными азиатами (p < 0,05).
Заключение. Различия аллельных вариантов и генотипов CYP3A4 и CYP3A5 в популяциях русских и якутов, больных лекарственно-устойчивым туберкулёзом лёгких, может существенно модифицировать клиническую эффективность и развитие нежелательных реакций при лечении бедаквилином, так в его окислении основное значение имеет изофермент CYP3A цитохрома Р450.
ISSN 2686-8849 (Online)