Перейти к:
Эффективность пропранолола у пациентов с циррозом печени и разными генотипами по полиморфному маркеру CYP2D6*4: серия случаев
https://doi.org/10.37489/2588-0527-2025-4-36-43
EDN: BBQDUA
Аннотация
В статье представлены два клинических наблюдения пациентов с циррозом печени и синдромом портальной гипертензии, получавших терапию неселективным β-адреноблокатором пропранололом. Цель сообщения — продемонстрировать влияние полиморфного маркера CYP2D6*4 (1846G>A) на гемодинамическую эффективность препарата. У пациента Б. (гетерозиготный генотип G/A1846) на фоне приёма пропранолола в дозе 30 мг/сут отмечено незначительное увеличение средней линейной скорости кровотока в воротной вене (СЛСКВ) — на 8,1 %, что расценено как недостаточный ответ. У пациента Г. (гомозиготный генотип G/G1846) в аналогичном режиме дозирования зарегистрировано выраженное увеличение СЛСКВ на 106,2 %. Таким образом, носительство нефункционального аллеля CYP2D6*4 ассоциировано с более низкой эффективностью пропранолола. Обсуждается целесообразность фармакогенетического тестирования перед назначением β-адреноблокаторов для персонализации терапии и профилактики кровотечений из варикозно-расширенных вен пищевода.
Ключевые слова
Для цитирования:
Сычев Д.А., Парусов А.И., Лоранская И.Д. Эффективность пропранолола у пациентов с циррозом печени и разными генотипами по полиморфному маркеру CYP2D6*4: серия случаев. Фармакогенетика и фармакогеномика. 2025;(4):36-43. https://doi.org/10.37489/2588-0527-2025-4-36-43. EDN: BBQDUA
For citation:
Sychev D.A., Parusov A.I., Loranskaya I.D. Propranolol efficacy in patients with liver cirrhosis and different polymorphic marker CYP2D6*4 genotypes. Pharmacogenetics and Pharmacogenomics. 2025;(4):36-43. (In Russ.) https://doi.org/10.37489/2588-0527-2025-4-36-43. EDN: BBQDUA
Введение
В последние годы отмечается стремительный рост числа больных циррозом печени. По статистическим данным Всемирной организации здравоохранения с 2020 года по сегодняшний день это заболевание входит в десятку основных причин мировой смертности, что характеризует данную патологию как грозную медико-социальную и экономическую проблему [1]. В Российской Федерации также с каждым годом регистрируется всё больше больных с диагнозом цирроз печени, установленным впервые в жизни, и к 2023 году это количество стойко достигло 80,1 на 100 тыс. населения страны, что превысило отметку аналогичного показателя 2020 года в 6 раз! [2].
Ключевым звеном патогенеза цирроза печени является синдром портальной гипертензии. Проявления этого симптомокомплекса разнообразны, самое ургентное и жизнеугрожающее из которых –– варикозное расширение вен пищевода и желудка, осложнённое кровотечением. В связи с этим в настоящее время проблема профилактики кровотечения из варикозно-расширенных вен является весьма актуальной. С этой целью в современные схемы терапии больных циррозом печени включены неселективные β‑адреноблокаторы (β-АБ), одним из которых является пропранолол. В клинических рекомендациях Российской гастроэнтерологической ассоциации по лечению больных циррозом печени рекомендовано назначать пропранолол в дозе, снижающей частоту пульса в покое на 25 % или до 55 ударов в минуту при исходно низком пульсе. Таким образом, доза препарата может варьировать от 10 до 320 мг в сутки и подбирается индивидуально [3].
Зарубежные гайдлайны до сих пор также не предлагают чёткого алгоритма назначения пропранолола. В последних на сегодняшний день клинических рекомендациях Европейской ассоциации по изучению печени (EASL) сказано, что применение неселективных β‑адреноблокаторов у пациентов с циррозом печени должно основываться на оценке соотношения риска/пользы для больного и его показателях центральной гемодинамики [4]. Кроме того, в ряде случаев β-адреноблокаторы не оказывают положительного гемодинамического эффекта.
Цитохром 2D6 (CYP2D6) является изоферментом цитохрома P450. Установлено, что CYP2D6 отвечает за метаболизм большого спектра лекарственных средств. К этим препаратам относятся и неселективные β‑адреноблокаторы, в том числе –– пропранолол [5]. Метаболизм последнего осуществляется за счёт реакции 4‑гидроксилирования [6]. Одна из особенностей CYP2D6 –– значительная вариабельность его активности в популяции. Основная причина вариабельности –– генетический полиморфизм, т. е. существование различных аллелей гена CYP2D6. Наиболее часто встречающиеся аллели CYP2D6 представлены следующими функциональными группами: с нормальной функцией (например, CYP2D6*1, *2 и *35), со сниженной функцией (например, CYP2D6*9, *10, *17, *29 и *41) и нефункциональные аллельные варианты (CYP2D6*3, *4, *6, *7, *8, *11, *12, *14, *15, *19, *20) [7].
В 2020 году нами проведено проспективное рандомизированное исследование, целью которого стала оптимизация эффективности фармакотерапии β-адреноблокаторами синдрома портальной гипертензии у больных циррозом печени с использованием фармакогенетических технологий [8]. В настоящей статье представлены два клинических примера пациентов, принявших участие в данном научном исследовании.
Цель
Продемонстрировать на клиническом примере различия эффективности пропранолола, определённой по динамике средней линейной скорости кровотока в воротной вене (СЛСКВ), у пациентов с циррозом печени и разными генотипами по полиморфному маркеру CYP2D6*4.
Материалы и методы
В проспективном рандомизированном исследовании, проведённом на клинической базе кафедры гастроэнтерологии ФГБОУ ДПО «Российская медицинская академия непрерывного профессионального образования» Минздрава Российской Федерации, приняло участие 60 пациентов с диагнозом цирроз печени.
Критерии включения в исследование: подтверждённый диагноз цирроза печени различной этиологии, класса А, В и С по Чайлд-Пью, возраст менее 75 лет и наличие подписанного пациентом информированного добровольного согласия на участие в исследовании и обработку персональных данных. Критериями невключения послужили наличие противопоказаний к применению пропранолола, регламентированных в инструкции по медицинскому применению препарата, утверждённой Министерством здравоохранения РФ; одновременный приём ингибиторов изофермента CYP2D6, лекарственных средств, метаболизм которых осуществляется посредством CYP2D6; перенесённое пациентом кровотечение из варикозно-расширенных вен пищевода во время настоящей госпитализации и сопутствующее онкологическое заболевание.
Для верификации диагноза цирроза печени использованы клинические (сбор жалоб и анамнеза, общий визуальный осмотр, измерение объёма живота, перкуссия и пальпация живота с определением размеров печени и селезёнки по Курлову) и лабораторные методы исследования (общие анализы крови и мочи, коагулограмма, биохимический анализ крови с определением уровня концентрации общего и прямого билирубина, аланинаминотрансферазы, аспартатаминотрансферазы, щелочной фосфатазы, лактатдегирдогеназы, гамма-глутамилтрансферазы, общего белка, альбумина, глюкозы, креатинина и мочевины). С целью оценки наличия или отсутствия осложнений, а также определения степени их выраженности проведены инструментальные методы исследования: ультрасонография органов брюшной полости с использованием допплерографии воротной вены. Произведено измерение размеров печени и селезёнки с описанием их эхо-структуры, диаметра и средней линейной скорости кровотока воротной вены, а также количества асцитической жидкости. За референтное значение средней линейной скорости кровотока воротной вены принималось 22,9±4,2 см/с [9]. Для выявления или исключения варикозного расширения вен пищевода, печёночной гастропатии и признаков кровотечения выполнена эзофагогастродуоденоскопия.
В целях определения динамики синдрома портальной гипертензии на фоне проводимой терапии пропранололом в дозе 10 мг 3 раза в сутки через 14 дней повторно использованы следующие ультрасонографические параметры: диаметр портальной вены и линейная скорость кровотока в портальной вене (аппарат ультразвуковой диагностики Toshiba Aplio 500). За критерий ответа на терапию пропранололом мы принимали любое увеличение СЛСКВ по сравнению с исходным. С целью оценки влияния полиморфизма гена CYP2D6*4 (1846G>A) на гемодинамический эффект пропранолола в рамках научного поиска в качестве критерия ответа принималось увеличение СЛСКВ на ≥10% и ≥20% по сравнению с исходным.
Венозную кровь пациентов собирали в первый день исследования в вакуумные пробирки с ЭДТА-К3 IMPROVACUTER (Guangzhou Improve Medical Instruments Co., Ltd, Китай). Выделение геномной ДНК из цельной крови осуществлялось с помощью набора реагентов S-Сорб для выделения ДНК на кремниевом сорбенте (ООО «Синтол», Россия). Носительство полиморфных маркеров CYP2D6*4 (1846G>A), определялось с помощью коммерческих наборов реагентов для определения соответствующих полиморфизмов (ООО «Синтол», Россия и «TaqMan®SNP Genotyping Assays» и TaqMan Universal Master Mix II, no UNG, Applied Biosystems, США) методом ПЦР в реальном времени на приборе CFX96 Touch Real Time System с ПО CFX Manager версии 3.0 (BioRad, США). Данное исследование проведено на базе научно-исследовательского института молекулярной и персонализированной медицины ФГБОУ ДПО «Российская медицинская академия непрерывного профессионального образования» Минздрава Российской Федерации.
Оценивая влияние полиморфизма гена CYP2D6*4 (1846G>A) на эффективность терапии пропранололом у пациентов с циррозом печени, построена унивариативная логистическая регрессионная модель. Вычисления осуществлялись на персональном компьютере с операционной системой Windows 10 Домашняя с использованием лицензионного программного продукта STATISTICA v10.0 («StatSoft Inc.», США).
Клиническое наблюдение
Клинический пример №1. Пациент Б., 63 лет. Госпитализирован по поводу декомпенсации цирроза печени.
При поступлении предъявлял жалобы на увеличение в объёме живота, снижение аппетита, одышку смешанного характера, возникающую в покое.
История заболевания: за один год до настоящей госпитализации установлен диагноз цирроз печени алкогольного генеза. В анамнезе –– лигирование вен пищевода по поводу их варикозного расширения 3 степени. Курсами принимает адеметионин и спиронолактон. Ухудшение самочувствия отмечает в течение недели, проявившееся в виде нарастания отёков нижних конечностей, увеличения в размерах живота и нарастающей одышки смешанного характера в покое, усиливающейся в положении лёжа.
По данным объективного осмотра пациента обращает на себя внимание бледность кожных покровов, иктеричность склер глаз, пальмарная эритема, симметричная пастозность обеих голеней и стоп, синусовая тахикардия до 96 ударов в минуту, тахипноэ с частотой дыхательных движений 20 в минуту. Язык сухой, негусто обложен налётом белого цвета по всей поверхности. Живот активно участвует в акте дыхания, увеличен в размерах (101 см) за счёт асцита, не напряжён. При пальпации безболезненный во всех отделах. Размеры печени по Курлову и селезёнки определить достоверно не представляется возможным ввиду асцита.
Лабораторно выявлены нарушение белково-синтетической функции печени в виде гипоальбуминемии, гипербилирубинемия в рамках печёночно-клеточной недостаточности. Маркеры вирусных гепатитов В и С в крови не обнаружены (табл. 1).
Таблица 1. Данные лабораторных исследований пациента
Общий анализ крови | |||||||||||||||||||
Эритроциты, 1012/л | Гемоглобин, г/л | Средний объём эритроцита (MCV), ед. | Лейкоциты, 109/л | Тромбоциты, 109/л | Скорость оседания эритроцитов, мм/час | ||||||||||||||
4,09 | 128 | 89 | 9,4 | 219 | 50 | ||||||||||||||
Общий анализ мочи | |||||||||||||||||||
Цвет | Относительная плотность | рН | Белок, г/л | Билирубин | Уробилиноген | Лейкоциты | Эритроциты | ||||||||||||
Жёлтый | 1026 | 5,0 | 0,1 | ++ | 1,0 | + | + | ||||||||||||
Биохимический анализ крови | |||||||||||||||||||
Общий белок, г/л | Альбумин, г/л | АЛТ, Ед/л | АСТ, Ед/л | Общий билирубин, мкмоль/л | Альфа-амилаза, Ед/л | Щелочная фосфатаза, Ед/л | |||||||||||||
81 | 23 | 19 | 50 | 33,3 | 90 | 234 | |||||||||||||
Коагулограмма | |||||||||||||||||||
МНО | Тромбиновое время, секунды | Протромбин по Квику, % | АЧТВ, секунды | Фибриноген, г/л | |||||||||||||||
1,35 | 16,7 | 45,1 | 36,6 | 2,4 | |||||||||||||||
Маркеры вирусных гепатитов | |||||||||||||||||||
HbsAg | анти-HCV | ||||||||||||||||||
Не обнаружен | Не обнаружен | ||||||||||||||||||
По данным ультразвукового исследования органов брюшной полости выявлено увеличение размеров печени: правая доля 165 мм, левая доля 88 мм. Характеристики печени: контуры чёткие, ровные, эхогенность значительно повышена, эхоструктура однородна, объёмных образований нет. Холедох не расширен. Интрапечёночные протоки не расширены. Диаметр воротной вены 15 мм. Средняя линейная скорость кровотока воротной вены 7,4 см/с. Индекс резистентности 0,17. Размер селезёнки 105х58 мм. Площадь селезёнки 45 см2. Объём селезёнки 215 см3. Свободная жидкость в брюшной полости определяется во всех отделах в большом количестве.
Таким образом, у больного ультрасонографически определяются признаки гепатомегалии, портальной гипертензии (в том числе значительное снижение средней линейной скорости кровотока воротной вены), асцита.
Эзофагогастродуоденоскопия: состояние после лигирования варикозно-расширенных вен пищевода.
На основании данных анамнеза, жалоб, физикального осмотра, лабораторного и инструментального обследования больному установлен диагноз:
Основное заболевание: цирроз печени алиментарной этиологии, класс B по Чайлд-Пью (8 баллов), 19 баллов по шкале MELD. Индекс Маддрея 25.87.
Осложнения основного заболевания: портальная гипертензия: состояние после эндоскопического лигирования варикозно-расширенных вен пищевода по поводу варикозного расширения вен пищевода 3 степени. Печёночно-клеточная недостаточность: гипоальбуминемия. Асцит 2 степени.
Пациенту проведено фармакогенетическое исследование –– детекция полиморфного маркера CYP2D6*4 (1846G>A) методом полимеразной цепной реакции в режиме реального времени. Определён гетерозиготный генотип G/A1846.
Больному назначена комплексная терапия: гепатопротекторная (урсодезоксихолевая кислота 500 мг в сутки), инфузионная (5% раствор глюкозы + 20% раствор рибоксина в объёма 500 мл в сутки), диуретическая (фуросемид 80 мг в сутки, спиронолактон 150 мг в сутки).
Для коррекции портальной гипертензии назначен пропранолол по 10 мг 3 раза в день per os.
Через 2 недели от начала терапии пропранололом при контрольном ультрасонографическом измерении средней линейной скорости кровотока воротной вены определено её незначительное увеличение до 8,0 см/с, то есть на 0,6 см/с или 8,1 % при сравнении с исходной СЛСКВ (рис. 1).
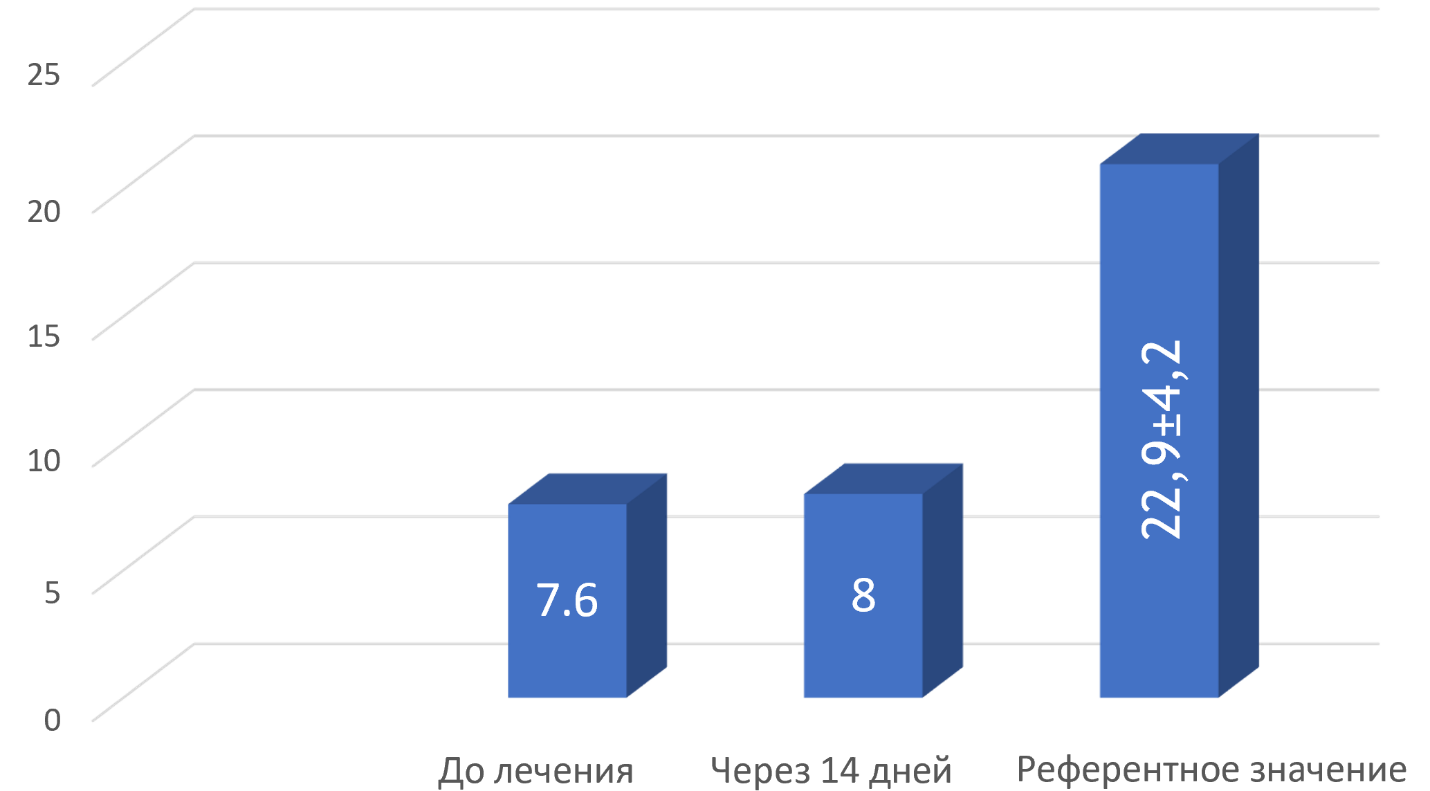
Рис. 1. Динамика средней линейной скорости кровотока воротной вены пациента и его референтное значение, см/с
Данный клинический пример свидетельствует о недостаточном терапевтическом эффекте (увеличение СЛСКВ менее, чем на 20 % от исходного) пропранолола у пациента с гетерозиготным генотипом G/A1846, что потребовало увеличения дозы препарата с учётом показателей центральной гемодинамики.
Клинический пример №2. Пациент Г., 42 лет.
Жалобы при поступлении на увеличение в объёме живота, снижение аппетита, тошноту, выраженную общую слабость.
Anamnesis morbi: ранее хроническими заболеваниями со стороны органов пищеварения не страдал, гастроэнтерологом не наблюдался. Настоящее ухудшение наступило в течение 10 дней до текущей госпитализации после недельного периода злоупотребления алкоголем.
При физикальном обследовании пациента выявлены иктеричность склер, пальмарная эритема, телеангиоэктазии на коже спины и передней поверхности грудной клетки, расширение подкожной венозной сети передней брюшной стенки. Отмечается заторможенная речь пациента (отвечает короткими предложениями с паузами). Язык малинового цвета, обложен налётом белого цвета у корня. Живот активно участвует в акте дыхания, обычной формы, не вздут. Пальпаторно мягкий, безболезненный во всех отделах. Размер печени по Курлову 12х11х10 см, край плотный, безболезненный при пальпации. Селезёнка размерами 10х7 см, при пальпации её край мягкий, безболезненный.
Лабораторно выявлены тромбоцитопения 1 степени, снижение уровня эритроцитов и биохимический синдром цитолиза умеренной степени, что отражает печёночно-клеточную недостаточность и синдром гиперспленизма. Макроцитоз эритроцитов указывает на алкогольный генез цирроза. Маркеры вирусных гепатитов В и С в крови не обнаружены (табл. 2).
Таблица 2. Данные лабораторных исследований пациента
Общий анализ крови | |||||||||||||||||||
Эритроциты, 1012/л | Гемоглобин, г/л | Средний объём эритроцита (MCV), ед. | Лейкоциты, 109/л | Тромбоциты, 109/л | Скорость оседания эритроцитов, мм/час | ||||||||||||||
3,96 | 134 | 102,9 | 9,7 | 121 | 56 | ||||||||||||||
Общий анализ мочи | |||||||||||||||||||
Цвет | Относительная плотность | рН | Белок, г/л | Билирубин | Уробилиноген | Лейкоциты | Эритроциты | ||||||||||||
Тёмно-жёлтый | 1026 | 5,5 | 0 | ++ | 2,0 | + | - | ||||||||||||
Биохимический анализ крови | |||||||||||||||||||
Общий белок, г/л | Альбумин, г/л | АЛТ, Ед/л | АСТ, Ед/л | Общий билирубин, мкмоль/л | Альфа-амилаза, Ед/л | ГГТП, Ед/л | |||||||||||||
85 | 38 | 65 | 150 | 68,3 | 63 | 2931 | |||||||||||||
Коагулограмма | |||||||||||||||||||
МНО | Тромбиновое время, секунды | Протромбин по Квику, % | АЧТВ, секунды | Фибриноген, г/л | |||||||||||||||
1,32 | 13,6 | 47,7 | 37,2 | 3,07 | |||||||||||||||
Маркеры вирусных гепатитов | |||||||||||||||||||
HbsAg | анти-HCV | ||||||||||||||||||
Не обнаружен | Не обнаружен | ||||||||||||||||||
Ультразвуковое исследование органов брюшной полости: печень –– правая доля
218 мм, левая доля 124 мм. Характеристики печени: контуры чёткие, ровные, эхогенность значительно повышена, эхоструктура однородна, объёмных образований нет. Холедох и интрапечёночные протоки не расширены. Диаметр воротной вены 12,3 мм. Средняя линейная скорость кровотока воротной вены 6,4 см/с. Индекс резистентности 0,52. Диаметр селезёночной вены 10 мм. Размер селезёнки 163х103 мм. Объём селезёнки 863 см3. Свободная жидкость в брюшной полости определяется межпетельно.
Таким образом, у пациента определяются ультрасонографические признаки гепатоспленомегалии, портальной гипертензии (в том числе значительное снижение средней линейной скорости кровотока воротной вены), асцита 1 степени.
Эзофагогастродуоденоскопия: варикозно-расширенные вены пищевода 2 степени, дуодено-гастральный рефлюкс.
На основании данных анамнеза, жалоб, физикального осмотра, лабораторного и инструментального обследования больному установлен диагноз:
Основное заболевание: цирроз печени алиментарной этиологии, класс B по Чайлд-Пью (8 баллов), 18 баллов по шкале MELD. Индекс Маддрея 13.65.
Осложнения основного заболевания: портальная гипертензия: спленомегалия с явлениями гиперспленизма, тромбоцитопения 1 степени. Варикозное расширение вен пищевода 2 степени. Печёночно-клеточная недостаточность: печёночная энцефалопатия 2 стадии. Асцит 1 степени.
Пациенту проведено фармакогенетическое исследование –– детекция полиморфного маркера CYP2D6*4 (1846G>A) методом полимеразной цепной реакции в режиме реального времени. Определён гомозиготный генотип G/G1846.
Больному назначена комплексная терапия: гепатопротекторная (урсодезоксихолевая кислота 1000 мг в сутки), инфузионная (0,9% раствор хлорида натрия в объёма 500 мл в сутки + 5% раствор калия хлорида 10 мл), диуретическая (фуросемид 20 мг в сутки, спиронолактон 100 мг в сутки) и гипоаммониемическая (суспензия лактулозы 30 мл в сутки per os).
С целью коррекции портальной гипертензии назначен пропранолол по 10 мг 3 раза в день per os.
При контрольном ультрасонографическом измерении средней линейной скорости кровотока воротной вены определено ее значительное увеличение до 13,2 см/с, то есть на 6,8 см/с или 106,2% при сравнении с исходной СЛСКВ (рис. 2).
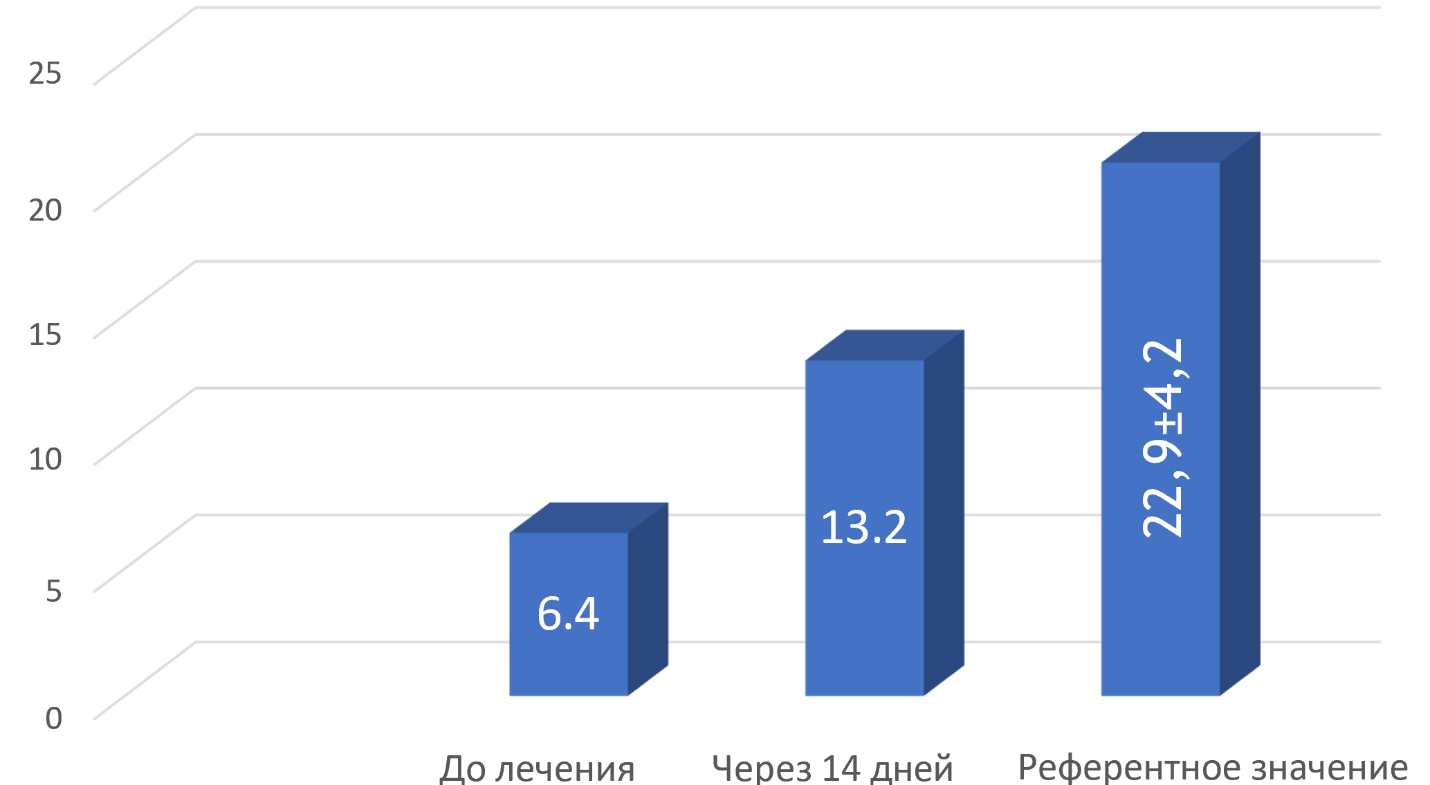
Рис. 2. Динамика средней линейной скорости кровотока воротной вены пациента и референтное значение, см/с
Таким образом, у больного с гомозиготным генотипом G/G1846 отмечается значительный положительный терапевтический эффект пропранолола (увеличение СЛСКВ более, чем на 20 % от исходного). Пациенту продолжена терапия в прежней дозе.
На рис. 3 представлено наглядное сравнение эффективности пропранолола, определённой по динамике средней линейной скорости кровотока воротной вены, у пациентов с циррозом печени и разными генотипами по CYP2D6*4.
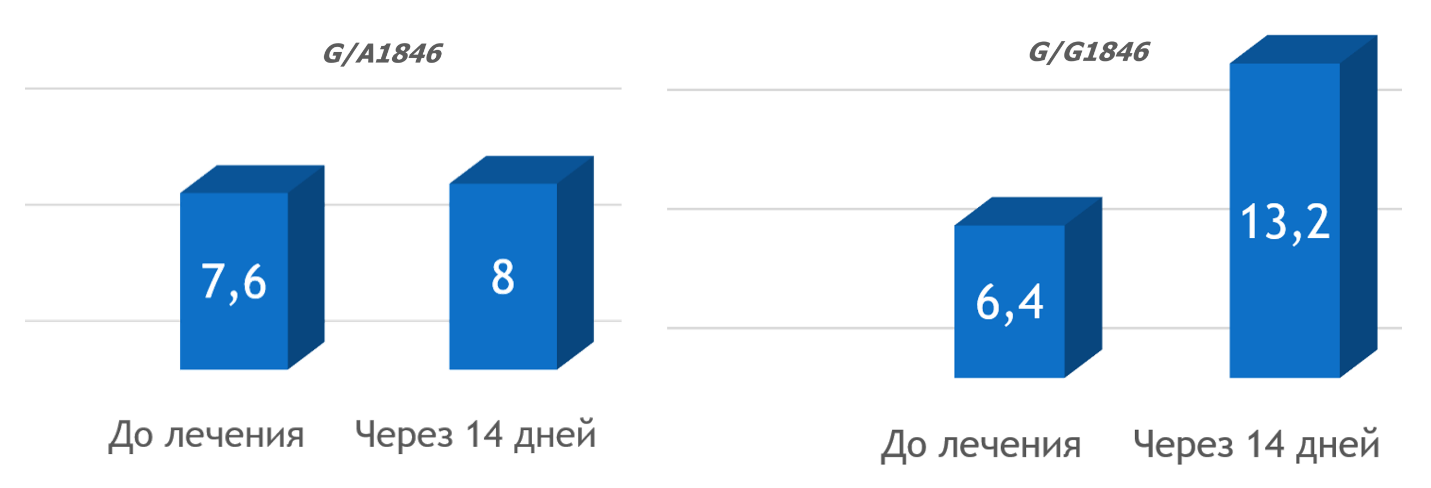
Рис. 3. Сравнение динамик средней линейной скорости кровотока воротной вены пациентов с разными генотипами по CYP2D6*4, см/с
Результаты
В результате нашего исследования установлено, что положительная динамика проявлений портальной гипертензии в виде увеличения СЛСКВ на 20 % и более от исходного на фоне терапии пропранололом чаще наблюдается у носителей гомозиготного генотипа CYP2D6 G/G1846 (89,7 %), чем у пациентов с гетерозиготным генотипом G/A1846 (10,3 %) в российской популяции (p <0,05).
Кроме того, нами впервые определён ультрасонографический критерий положительной динамики течения портальной гипертензии в виде увеличения СЛСКВ на 20 % и более от исходного на фоне терапии пропранололом (p <0,05).
По результатам проведённого фармакогенетического исследования разработан алгоритм персонализации лечения пациентов с циррозом печени неселективными
β-адреноблокаторами (рис. 4).
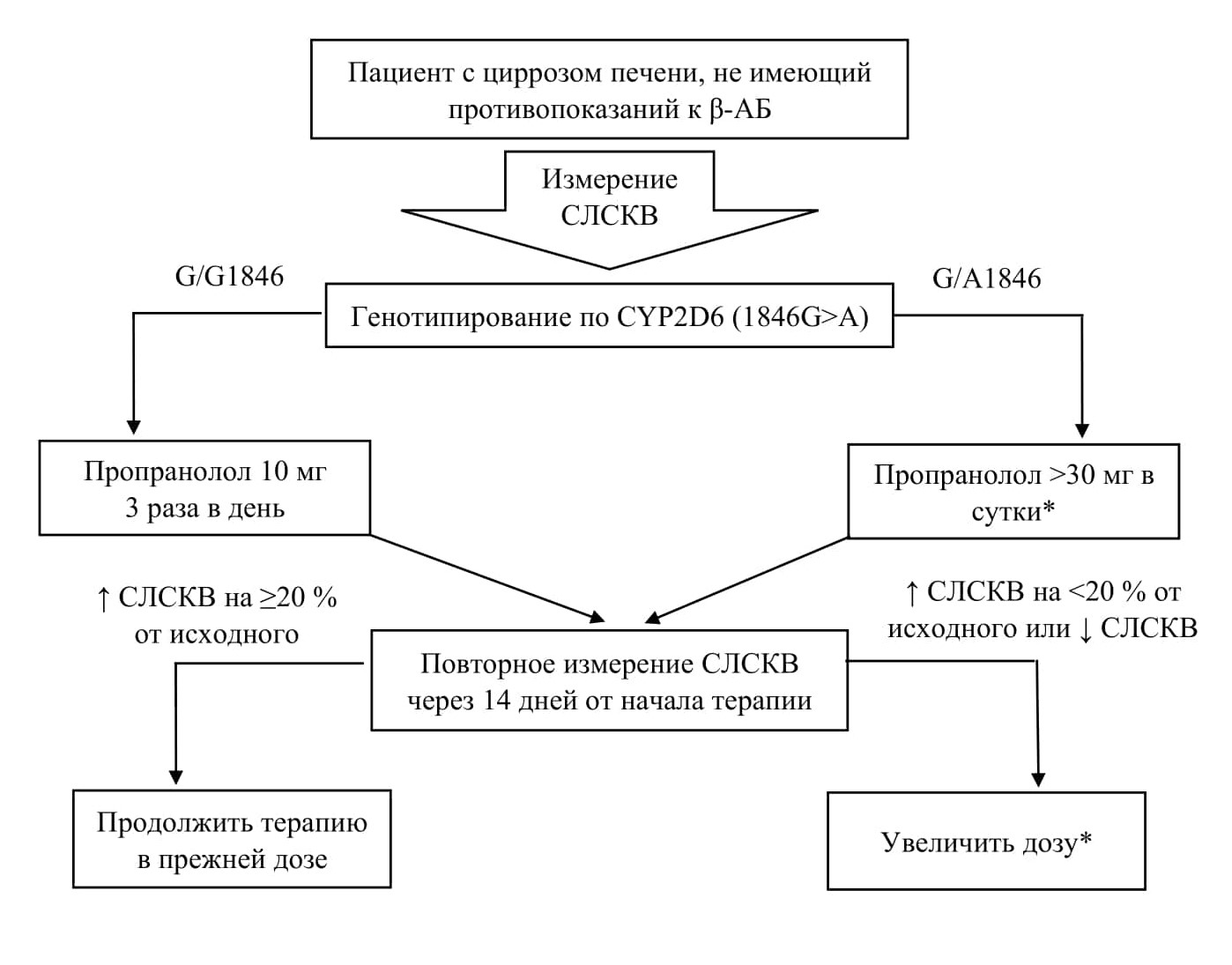
Рис. 4. Алгоритм персонализации лечения пациентов с циррозом печени неселективными β-адреноблокаторами
Примечание: *Пропранолол назначать в дозе, снижающей ЧСС на 25% в покое или до 55 ударов в минуту при брадикардии.
Для достижения положительного гемодинамического эффекта пациентам с гомозиготным генотипом G/G1846 следует начинать терапию пропранололом в дозе 10 мг 3 раза в день. Носителям гетерозиготного генотипа G/A1846 –– назначать дозу выше 30 мг в сутки. Для контроля терапии требуется ультрасонографическая оценка динамики средней линейной скорости кровотока воротной вены. При наблюдении положительного гемодинамического эффекта по изменению СЛСКВ необходимо продолжить назначение пропранолола в прежней дозе, в противном случае –– увеличивать дозу индивидуально, учитывая показатели центральной гемодинамики согласно актуальным клиническим рекомендациям, утверждённым Министерством здравоохранения Российской Федерации, по диагностике и лечению цирроза печени (2021 г.) [3].
Заключение
Данные клинические примеры наглядно демонстрируют различия эффективности пропранолола у пациентов с циррозом печени и разными генотипами по полиморфному маркеру CYP2D6*4.
Соблюдение предложенного алгоритма персонализации лечения пациентов с циррозом печени неселективными β-адреноблокаторами актуально для профилактики развития кровотечения из варикозно-расширенных вен пищевода, как одного из наиболее грозных осложнений цирроза печени. Результаты нашего исследования внедрены в клиническую практику.
Список литературы
1. World health statistics 2024: Monitoring health for the SDGs, Sustainable Development Goals World Health Organization. 2024 May; Suppl 1: 14. Режим доступа: https://iris.who.int/bitstream/handle/10665/376869/9789240094703
2. Заболеваемость всего населения России в 2023 году. Статистические материалы. Министерство здравоохранения Российской Федерации. Департамент мониторинга, анализа и стратегического развития здравоохранения. ФГБУ «Центральный научно-исследовательский институт организации и информатизации здравоохранения» Минздрава России. 2024; часть II: 114. [Morbidity of the entire population of Russia in 2023. Statistical materials. Ministry of Health of the Russian Federation. Department of Monitoring, Analysis and Strategic Development of Healthcare. Federal State Budgetary Institution "Central Research Institute for Healthcare Organization and Informatization" of the Ministry of Health of the Russian Federation. 2024; Part II: 114. (In Russ.)]. Режим доступа: https://www.niig.su/images/documents/sgm/regions/02_Общая_заболеваемость_всего_населения_России_в_2023_году.
3. Ивашкин В.Т., Маевская М.В., Жаркова М.С., и др. Клинические рекомендации Российского общества по изучению печени и Российской гастроэнтерологической ассоциации по диагностике и лечению фиброза и цирроза печени и их осложнений. Российский журнал гастро энтерологии, гепатологии, колопроктологии. 2021;31(6):56-102. [Ivashkin V.T., Maevskaya M.V., Zharkova M.S., et al. Clinical Recommendations of the Russian Scientific Liver Society and Russian Gastroenterological Association on Diagnosis and Treatment of Liver Fibrosis, Cirrhosis and Their Complications. Russian Journal of Gastroenterology, Hepatology, Coloproctology. 2021;31(6):56-102. (In Russ.)].
4. European Association for the Study of the Liver. EASL Clinical Practice Guidelines for the management of patients with decompensated cirrhosis. J Hepatol. 2018 Aug;69(2):406-460. doi: 10.1016/j.jhep.2018.03.024. Epub 2018 Apr 10. Erratum in: J Hepatol. 2018 Nov;69(5):1207. doi: 10.1016/j.jhep.2018.08.009.
5. Абдрашитов Р.Х., Гильдеева Г.Н., Раменская Г.В., Смирнов В.В. Обзор существующих методик оценки активности CYP2D6 с применением экзогенных и эндогенных маркеров. Фармакокинетика и Фармакодинамика. 2015;(1):4-11. [Abdrashitov A.D., Gildeeva G.N., Ramenskaya G.V., Smirnov V.V. Review of existing methodologies to assess the activity of CYP2D6 using exogenous and endogenous markers. Pharmacokinetics and Pharmacodynamics. 2015;(1):4-11. (In Russ.)].
6. Wu X, Yuan L, Zuo J, et al. The impact of CYP2D6 polymorphisms on the pharmacokinetics of codeine and its metabolites in Mongolian Chinese subjects. Eur J Clin Pharmacol. 2014 Jan;70(1):57-63. doi: 10.1007/s00228-013-1573-x.
7. Sheridan RP, Korzekwa KR, Torres RA, Walker MJ. Empirical regioselectivity models for human cytochromes P450 3A4, 2D6, and 2C9. J Med Chem. 2007 Jul 12;50(14):3173-84. doi: 10.1021/jm0613471.
8. Сычев Д.А., Парусов А.И., Лоранская И.Д., и др. Роль полиморфных маркеров гена CYP2D6 в определении оптимальной тактики лечения портальной гипертензии у больных циррозом печени. Терапевтический архив. 2022;94(2):200–208. [Sychev D.A., Parusov A.I., Loranskaya I.D., et al. The role of polymorphic markers of the CYP2D6 gene in determining the optimal treatment tactics for portal hypertension in patients with liver cirrhosis. Therapeutic archive. 2022;94(2):200–208. (In Russ.)] doi: 10.26442/00403660.2022.02.201371.
9. Допплерография в диагностике заболеваний печени, желчного пузыря, поджелудочной железы и их сосудов / В. В. Митьков. М. : Видар-М, 2000. 146 с. ил., цв. ил.; 21. ISBN 5-88429-056-Х. [Dopplerography in diagnostics of diseases of the liver, gall bladder, pancreas and their vessels / V. V. Mitkov. M.: Vidar-M, 2000. 146 p. ill., color ill.; 21. ISBN 5-88429-056-X. (In Russ.)].
Об авторах
Д. А. СычевРоссия
Сычев Дмитрий Алексеевич — д. м. н., профессор, профессор РАН, академик РАН, научный руководитель Центра геномных исследований мирового уровня «Центр предиктивной генетики, фармакогенетики и персонализированной терапии» ФГБНУ «Российский научный центр хирургии имени академика Б.В. Петровского»; зав. кафедрой клинической фармакологии и терапии имени Б.Е. Вотчала
А. И. Парусов
Россия
Парусов Андрей Игоревич — к. м. н., доцент кафедры гастроэнтерологии
И. Д. Лоранская
Россия
Лоранская Ирина Дмитриевна — д. м. н., профессор, зав. кафедрой гастроэнтерологии, декан терапевтического факультета
Что уже известно об этой теме?
Проблема: цирроз печени и его осложнение — портальная гипертензия (варикозное расширение вен пищевода, угроза кровотечения) — являются значимой причиной смертности.
Стандартная терапия: для снижения давления в воротной вене и профилактики кровотечений применяются неселективные бета-адреноблокаторы, такие как пропранолол. Доза подбирается индивидуально, в основном по частоте пульса, но четкого алгоритма нет, и у части пациентов препарат недостаточно эффективен.
Роль генетики: известно, что пропранолол метаболизируется в печени ферментом CYP2D6. Активность этого фермента зависит от генетических полиморфизмов (вариантов гена CYP2D6), в частности, наличие нефункционального аллеля CYP2D6*4 снижает скорость метаболизма препарата.
Что нового даёт статья?
Конкретные клинические примеры: статья наглядно демонстрирует на двух пациентах с циррозом, как генетические различия влияют на эффективность терапии:
Пациент Б. (генотип G/A, носитель одного нефункционального аллеля): на стандартной дозе пропранолола (30 мг/сут) скорость кровотока в воротной вене (СЛСКВ) увеличилась незначительно — всего на 8,1%. Это расценено как недостаточный ответ.
Пациент Г. (генотип G/G, нормальный функциональный аллель): на той же дозе препарата скорость кровотока увеличилась значительно — на 106,2%, что говорит о высокой эффективности.
Подтверждение гипотезы: работа подтверждает, что носительство нефункционального аллеля CYP2D6*4 (гетерозиготный генотип G/A) ассоциировано с более низкой гемодинамической эффективностью пропранолола у пациентов с циррозом печени.
Предложен критерий оценки: авторы предлагают использовать ультразвуковой критерий эффективности — увеличение средней линейной скорости кровотока в воротной вене (СЛСКВ) на 20% и более от исходного уровня на фоне терапии.
Как это может повлиять на клиническую практику в обозримом будущем?
Персонализация терапии: результаты обосновывают целесообразность проведения фармакогенетического тестирования на полиморфизм CYP2D6*4 до назначения пропранолола.
Алгоритм назначения: предложен конкретный алгоритм действий:
Генотип G/G: начинать терапию со стандартной дозы (30 мг/сут) и контролировать эффект по СЛСКВ.
Генотип G/A (носители «медленного» аллеля): изначально назначать более высокие дозы препарата (выше 30 мг/сут) для достижения клинически значимого эффекта, так как стандартная доза у них неэффективна.
Повышение эффективности профилактики: такой подход позволит заранее выявить пациентов, которые с высокой вероятностью не ответят на стандартную терапию, и скорректировать дозу или тактику ведения для снижения риска опасных кровотечений из вен пищевода.
Рецензия
Для цитирования:
Сычев Д.А., Парусов А.И., Лоранская И.Д. Эффективность пропранолола у пациентов с циррозом печени и разными генотипами по полиморфному маркеру CYP2D6*4: серия случаев. Фармакогенетика и фармакогеномика. 2025;(4):36-43. https://doi.org/10.37489/2588-0527-2025-4-36-43. EDN: BBQDUA
For citation:
Sychev D.A., Parusov A.I., Loranskaya I.D. Propranolol efficacy in patients with liver cirrhosis and different polymorphic marker CYP2D6*4 genotypes. Pharmacogenetics and Pharmacogenomics. 2025;(4):36-43. (In Russ.) https://doi.org/10.37489/2588-0527-2025-4-36-43. EDN: BBQDUA
JATS XML











































