Перейти к:
Оптимизация терапии тамоксифеном: значение фармакогенетического тестирования для улучшения приверженности лечению
https://doi.org/10.37489/2588-0527-2025-1-36-40
EDN: CJHUHQ
Аннотация
Тамоксифен остаётся золотым стандартом эндокринной терапии у пациенток с раком молочной железы (РМЖ), положительным по рецепторам к эстрогенам. Однако его эффективность напрямую зависит от приверженности лечению, которая часто снижается из-за нежелательных лекарственных реакций и индивидуальных различий в метаболизме препарата. В статье представлены данные исследования приверженности терапии тамоксифеном через 5 лет наблюдения во взаимосвязи с выявленными раннее фармакогенетическими ассоциациями с возникновением нежелательных лекарственных реакций. Фармакогенетическое тестирование перед назначением тамоксифена может улучшить приверженность лечения за счёт персонализации терапии и снижения частоты нежелательных лекарственных явлений.
Ключевые слова
Для цитирования:
Голубенко Е.О., Савельева М.И., Коренная В.В. Оптимизация терапии тамоксифеном: значение фармакогенетического тестирования для улучшения приверженности лечению. Фармакогенетика и фармакогеномика. 2025;(1):36-40. https://doi.org/10.37489/2588-0527-2025-1-36-40. EDN: CJHUHQ
For citation:
Golubenko E.O., Savelyeva M.I., Korennaya V.V. Optimizing tamoxifen therapy: the importance of pharmacogenetic testing to improve adherence. Pharmacogenetics and Pharmacogenomics. 2025;(1):36-40. (In Russ.) https://doi.org/10.37489/2588-0527-2025-1-36-40. EDN: CJHUHQ
Введение
Тамоксифен остаётся золотым стандартом эндокринной терапии у пациенток с раком молочной железы (РМЖ), положительным по рецепторам к эстрогенам. Однако его эффективность напрямую зависит от приверженности лечению, которая часто снижается из-за нежелательных лекарственных реакций и индивидуальных различий в метаболизме препарата. Фармакогенетические исследования позволяют прогнозировать ответ на терапию тамоксифеном и оптимизировать лечение.
Приверженность к длительной (5–10 лет) терапии тамоксифеном остаётся недостаточной: по данным исследований, до 50 % пациенток снижают дозу или прекращают лечение. Основные причины:
- Нежелательные лекарственные реакции (НЛР): приливы, тамоксифен-индуцированные альтерации эндометрия, боли в костях и суставах, астения, тромбоэмболии [1].
- Психологические факторы (депрессия, тревога, забывчивость) [2].
- Недостаточная информированность о важности длительного приёма.
Тамоксифен является пролекарством, его активный метаболит — эндоксифен — образуется под действием фермента CYP2D6. Полиморфизмы гена CYP2D6 могут значительно влиять на концентрацию эндоксифена. Для ультрабыстрых метаболизаторов свойственен высокий уровень эндоксифена, больше риск развития НЛР, а для промежуточных и медленных — сниженная эффективность, больший риск рецидива [3].
Помимо CYP2D6, важную роль играют полиморфные варианты генов CYP3A5*3, CYP2C9*2, CYP2C9*3, CYP2C19*2, CYP2C19*3 и ABCB1.
В течение пяти лет, с 2017 по 2022 год, нами было выполнено когортное клиническое исследование, включавшее три этапа. Начальный этап, реализованный в 2017 году, представлял собой ретроспективный анализ клинических и эпидемиологических данных для определения частоты встречаемости и факторов риска развития гиперплазии эндометрия у пациенток с РМЖ, состоящих на учёте в онкологических учреждениях Москвы (n=230) [18].
Второй этап был посвящён фармакогенетическому исследованию, направленному на изучение клинических проявлений НЛР эндокринной терапии тамоксифеном и оценку корреляции между наличием полиморфных вариантов генов, кодирующих ферменты системы цитохрома P-450 и белки-транспортеры лекарств, и возникновением НЛР у пациенток с РМЖ. В данном этапе приняли участие 120 женщин с РМЖ, которым было проведено генетическое тестирование полиморфных вариантов генов ферментов системы цитохрома Р-450 и гликопротеина-Р (Рg).
Ассоциативный анализ выявил взаимосвязь между данными полиморфизмами и развитием НЛР на тамоксифен, что указывает на клиническую значимость генетических полиморфизмов CYP2D6, CYP3A5, CYP2C9 и ABCB1 [4, 5]. Далее нами была исследована приверженность к терапии тамоксифеном через 5 лет наблюдения во взаимосвязи с выявленными раннее фармакогенетическими ассоциациями.
Материал и методы
В данном исследовании, основанном на анкетировании, приняли участие 54 пациентки, ранее проходившие фармакогенетическое исследование, страдающие РМЖ. Сбор данных осуществлялся посредством телефонных интервью или электронных анкет. Предложенная анкета включала вопросы, касающиеся частоты посещений онколога и гинеколога в течение пятилетнего периода приёма тамоксифена. В связи с ограниченным объёмом выборки, для анализа выявленных различий применялся метод дельта-процентов (∆%) с установленным порогом значимости в 5 %. Выявленные раннее результаты фармакогенетического исследования были учтены при интерпретации данных, полученных в ходе настоящего опросного исследования [4, 5].
Результаты и их обсуждение
В исследовании приняли участие 54 пациентки, что составляет 45 % от общего числа респондентов. У 9,26 % участниц (n=5) было зафиксировано прогрессирование заболевания (из этой подгруппы 4 пациентки самопроизвольно отменили приём тамоксифена, одна пациентка чётко следовала режиму терапии); в то время как у 90,74 % (рис. 1) болезнь не прогрессировала. Большинство опрошенных, а именно 59,26 % (n=32), продолжают терапию тамоксифеном в прежней дозировке и без перерывов. Оставшиеся 40,74 % (n=22) прекратили приём тамоксифена. В этой группе 9 пациенток перешли на альтернативное лечение, используя ингибиторы ароматазы, а 13 самостоятельно прекратили приём препарата из-за непереносимости.
За исключением тамоксифен-индуцированных альтераций эндометрия, частота возникновения побочных эффектов лекарственных средств была выше в группе пациенток, прекративших приём тамоксифена (табл. 1).
Таблица 1
Сравнение нежелательных лекарственных реакции тамоксифена в двух группах пациенток с раком молочной железы: продолжающих и прекративших приём препарата
Нежелательная лекарственная реакция | Продолжают терапию тамоксифеном, n (%) | Прекратили приём тамоксифена, n (%) | ∆% |
Тамоксифен-индуцированные альтерации эндометрия | 7 (21,88 %) | 4 (18,18 %) | 3,7 |
Приливы | 21 (65,63 %) | 17 (77,27 %) | -11,64 |
Астения | 15 (46,88 %) | 12 (54,55 %) | -7,67 |
Боли в костях | 15 (46,88 %) | 12 (54,55 %) | -7,67 |
Диспепсия | 5 (15,63 %) | 2 (22,22 %) | -6,59 |
Всего | 32 (100 %) | 22 (100 %) | 0 |
На протяжении пятилетнего периода мониторинга, установлено, что 57,4 % обследуемых (общее число — 31) посещали акушера-гинеколога с частотой не менее одного раза в год, в то время как 42,59 % (n=23) обращались за гинекологической помощью реже одного раза в год.
Отмечено существенное различие в регулярности наблюдения у акушера-гинеколога между группами пациенток. В группе пациенток, продолжающих терапию тамоксифеном, 75 % (n=24) регулярно наблюдались у акушера-гинеколога. В противоположность этому, в группе пациенток, прекративших приём тамоксифена, лишь 31,82 % (n=7) соблюдали регулярность посещений. Примечательно, что в подгруппе пациенток, прекративших приём тамоксифена из-за его плохой переносимости (n=13), регулярность наблюдения была наименьшей, составив 7,69 %.
Из тринадцати пациенток (100 %), самостоятельно прекративших терапию тамоксифеном из-за неблагоприятной переносимости, у десяти (76,92 %) наблюдались приливы. При этом у семи из них (53,85 %) был обнаружен генотип GG полиморфного варианта CYP2D6*4. Астения была зафиксирована у восьми участниц (61,54 %), и у семи из них (53,85 %) выявлен гомозиготный референсный генотип 42614AА по rs1057910 гена CYP2C9.
В указанной подгруппе, гиперплазия эндометрия в процессе лечения была диагностирована у четырёх женщин (30,77 %), а генотип ТТ полиморфного варианта АВСВ1 3435T>C был выявлен только у одной пациентки (7,69 %). Семь пациенток (53,85 %) жаловались на костные боли; у четырёх из них (30,77 %) обнаружен генотип GG полиморфного варианта CYP2D6*4, у такого же количества (30,77 %) — генотип СТ полиморфного варианта АВСВ1 3435T>C, у всех пациенток этой группы (53,85 %) выявлен генотип АА полиморфного варианта CYP2C9*3. По полученным данным, указанные полиморфные варианты демонстрируют статистически значимую связь с возникновением болей в костях. Диспепсические явления наблюдались у шести пациенток (46,15 %), причём у четырёх (30,77 %) был генотип ТТ полиморфного варианта АВСВ1 3435T>C (рис. 1).
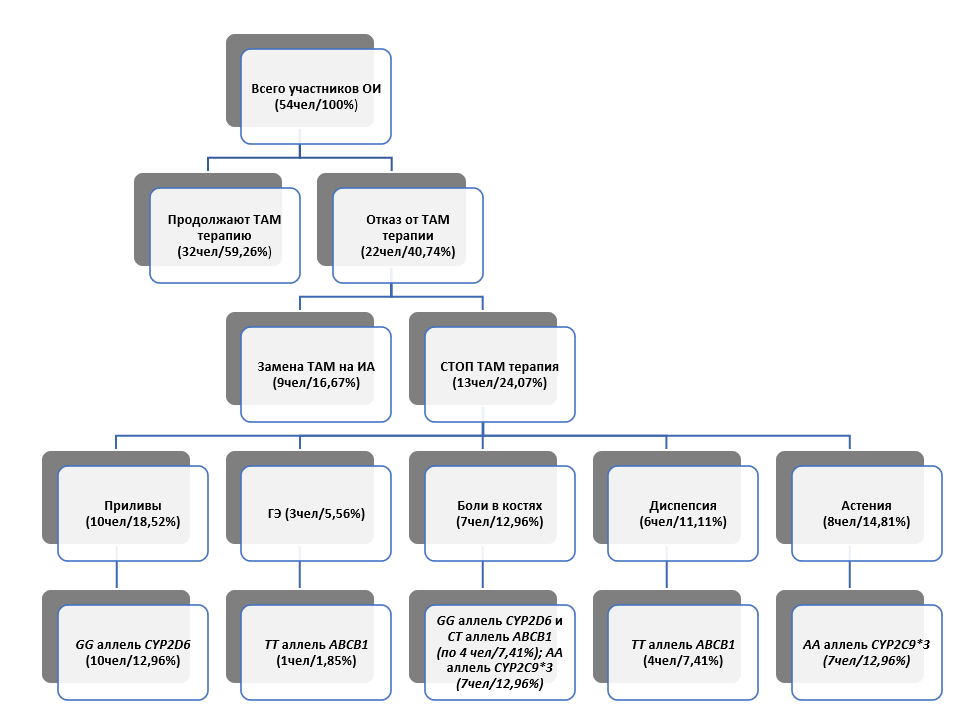
Рис. 1. Результаты исследования приверженности лечению во взаимосвязи с наличием полиморфных вариантов генов системы цитохрома Р-450 и гена АВСВ1
Примечания: ОИ — опросное исследование; ТАМ — тамоксифен; СТОП ТАМ — прекращение терапии тамоксифеном; ГЭ — гиперплазия эндометрия; ИА — ингибиторы ароматазы.
Во всех анализируемых группах пациенток прослеживается закономерность: более выраженные НЛР тамоксифена чаще возникают у лиц с определёнными генетическими вариациями. Эти полиморфизмы затрагивают гены, ответственные за синтез ферментов цитохрома P-450 и транспортных белков, участвующих в метаболизме лекарственных препаратов.
Заключение
Клиническое применение фармакогенетики для повышения приверженности возможно в следующих аспектах:
- Персонализация дозы — увеличение дозы у медленных метаболизаторов или переход на ингибиторы ароматазы у пациенток с высоким риском неэффективности.
- Прогнозирование токсичности — предотвращение отмены препарата из-за НЛР.
- Обучение пациенток — объяснение генетических причин индивидуального ответа на терапию повышает мотивацию к соблюдению режима приёма [6].
Таким образом, фармакогенетическое тестирование перед назначением тамоксифена может улучшить приверженность лечению за счёт персонализации терапии и снижения частоты нежелательных лекарственных явлений. Внедрение генетического скрининга в клиническую практику требует дальнейших исследований, но уже сейчас способно повысить приверженность лечению РМЖ.
Список литературы
1. Drullinsky PR, Hurvitz SA. Mechanistic basis for PI3K inhibitor antitumor activity and adverse reactions in advanced breast cancer. Breast Cancer Res Treat. 2020 Jun;181(2):233-248. doi: 10.1007/s10549-020-05618-1.
2. Kolberg HC, Jackisch C, Hurvitz SA, et al. Is weight-based IV dosing of trastuzumab preferable to SC fixed-dose in some patients? A systematic scoping review. Breast. 2021 Jun;57:95-103. doi: 10.1016/j.breast.2021.03.003.
3. Chan CWH, Law BMH, So WKW, et al. Pharmacogenomics of breast cancer: highlighting CYP2D6 and tamoxifen. J Cancer Res Clin Oncol. 2020 Jun;146(6):1395-1404. doi: 10.1007/s00432-020-03206-w.
4. Голубенко Е.О., Савельева М.И., Созаева Ж.А., и др. Клиническое значение генетического полиморфизма ферментов метаболизма и транспортеров тамоксифена при раке молочной железы: результаты популяционного когортного исследования. Фарматека. 2022;29(11-12):118-126. doi: 10.18565/pharmateca.2022.11-12.118-126.
5. Голубенко Е.О., Савельева М.И., Созаева Ж.А., и др. Прогностическое моделирование нежелательных лекарственных реакций тамоксифена при раке молочной железы (результаты когортного исследования). Фармакогенетика и фармакогеномика. 2022;(1):63-73. doi: 10.37489/2588-0527-2022-1-63-73.
6. Bolhuis K, Bond MJG, Van Amerongen MJ, et al; Dutch Colorectal Cancer Group Liver Expert Panel. The role of tumour biological factors in technical anatomical resectability assessment of colorectal liver metastases following induction systemic treatment: An analysis of the Dutch CAIRO5 trial. Eur J Cancer. 2023 Apr;183:49-59. doi: 10.1016/j.ejca.2023.01.013.
Об авторах
Е. О. ГолубенкоРоссия
Екатерина Олеговна Голубенко, ассистент
кафедра акушерства и гинекологии
Москва
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов
М. И. Савельева
Россия
Марина Ивановна Савельева, д. м. н., профессор,
профессор кафедры
кафедра терапии имени Е.Н. Дормидонтова
Ярославль
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов
В. В. Коренная
Россия
Вера Вячеславовна Коренная, к. м. н., доцент
кафедра акушерства и гинекологии
Москва
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов
Что уже известно об этой теме?
Тамоксифен — «золотой стандарт» эндокринной терапии при ER+ раке молочной железы (РМЖ).
Его эффективность напрямую зависит от приверженности лечению (приему препарата в течение 5-10 лет).
Приверженность часто снижается (до 50% пациенток) из-за нежелательных лекарственных реакций (НЛР): приливы, поражения эндометрия, боли в костях, астения.
Тамоксифен — пролекарство, его активация зависит от фермента CYP2D6. Известно, что генетические полиморфизмы (в генах CYP2D6, CYP2C9, CYP3A5, ABCB1 и др.) влияют на скорость метаболизма препарата, что может определять как его эффективность, так и риск развития НЛР.
Что нового даёт статья?
Статья предоставляет новые клинические данные о связи между конкретными генетическими вариантами, развитием НЛР и фактической приверженностью лечению через 5 лет.
Подтверждено, что у пациенток, самостоятельно прекративших прием тамоксифена из-за непереносимости, достоверно чаще встречаются определенные генотипы (например, *CYP2D6*4* GG ассоциирован с приливами, а *CYP2C9*3* AA — с болями в костях).
Выявлена важная корреляция: пациентки, которые продолжали терапию, значительно чаще (75% vs 31.82%) регулярно наблюдались у гинеколога, что подчеркивает роль врачебного контроля в приверженности.
Как это может повлиять на клиническую практику в обозримом будущем?
Внедрение фармакогенетического тестирования до назначения тамоксифена может стать рутинной практикой для персонализации терапии:
Коррекция дозы для пациенток с медленным метаболизмом.
Своевременный переход на ингибиторы ароматазы у тех, кто имеет высокий генетический риск неэффективности или тяжелых НЛР от тамоксифена.
Прогнозирование и объяснение НЛР: возможность заранее предупредить пациентку о вероятных побочных эффектах и их генетической природе повысит мотивацию к продолжению лечения и предотвратит самовольную отмену препарата.
Улучшение приверженности: персонализированный подход на основе генетики позволит повысить приверженность лечению, что напрямую повлияет на снижение риска рецидивов и повышение выживаемости пациенток с РМЖ.
Рецензия
Для цитирования:
Голубенко Е.О., Савельева М.И., Коренная В.В. Оптимизация терапии тамоксифеном: значение фармакогенетического тестирования для улучшения приверженности лечению. Фармакогенетика и фармакогеномика. 2025;(1):36-40. https://doi.org/10.37489/2588-0527-2025-1-36-40. EDN: CJHUHQ
For citation:
Golubenko E.O., Savelyeva M.I., Korennaya V.V. Optimizing tamoxifen therapy: the importance of pharmacogenetic testing to improve adherence. Pharmacogenetics and Pharmacogenomics. 2025;(1):36-40. (In Russ.) https://doi.org/10.37489/2588-0527-2025-1-36-40. EDN: CJHUHQ
JATS XML











































