Перейти к:
Прогностическое моделирование нежелательных лекарственных реакций тамоксифена при раке молочной железы (результаты когортного исследования)
https://doi.org/10.37489/2588-0527-2022-1-63-73
Аннотация
Актуальность. Эндокринная терапия — стандартный метод лечения женщин с ER-положительным раком молочной железы (РМЖ). Примерно у 30 % пациентов с РМЖ будет рецидив заболевания в течение 15 лет после лечения, что указывает на широкую вариабельность клинического ответа на лечение тамоксифеном. В статье представлены результаты проспективного фармакогенетического когортного исследования, проводившегося в 2018–2019 годах. Цель. Провести анализ нежелательных лекарственных реакций тамоксифена в адъювантном режиме у пациенток с РМЖ во взаимосвязи с носительством генетических полиморфизмов генов, кодирующих ферменты цитохромной системы Р450 и белки-транспортёры лекарственных средств, и построение на их основе прогностических моделей. Материалы и методы. В исследовании участвовали 120 женщин с РМЖ, прошедшие генетическое тестирование на полиморфизмы генов ферментов цитохрома P450 (CYP) и транспортёров Р-гликопротеина (Pg). Критерии включения: гистологически подтверждённый диагноз РМЖ, приём тамоксифена в рекомендуемых дозах, установление диагноза не ранее 2007 года, получение информированного добровольного согласия на участие в исследовании. Аллельные варианты определялись с помощью метода полимеразной цепной реакции в режиме реального времени в Научно-исследовательском институте молекулярной и персонализированной медицины ФГБОУ ДПО РМАНПО Минздрава России. Результаты. В результате ассоциативного анализа показана связь генетических полиморфизмов CYP2D6, CYP3A5, CYP2C9 и ABCB1 с развитием нежелательных лекарственных реакций (НЛР) тамоксифена, свидетельствующая об их клинической значимости. Проведённый комплексный ассоциативный анализ позволил с использованием математического моделирования построить прогностические модели риска развития таких НЛР при приёме ТАМ, как приливы, диспепсия, боли в костях и астения. Полученные регрессионные модели были статистически значимы (p < 0,001) и продемонстрировали высокую диагностическую эффективность, что позволяет имплементировать их в клиническую практику. Заключение. Таким образом, модели, включающие как генетические, так и негенетические детерминанты, могут способствовать дальнейшему улучшению предсказания индивидуального ответа на тамоксифен у пациенток с РМЖ.
Ключевые слова
Для цитирования:
Голубенко Е.О., Савельева М.И., Созаева Ж.А., Поддубная А.В., Коренная В.В. Прогностическое моделирование нежелательных лекарственных реакций тамоксифена при раке молочной железы (результаты когортного исследования). Фармакогенетика и фармакогеномика. 2022;(1):63-73. https://doi.org/10.37489/2588-0527-2022-1-63-73
For citation:
Golubenko E.O., Savelyeva M.I., Sozaeva Z.A., Poddubnaya I.V., Korennaya V.V. Predictive modeling of adverse events of tamoxifen therapy for breast cancer (results of a cohort study). Pharmacogenetics and Pharmacogenomics. 2022;(1):63-73. (In Russ.) https://doi.org/10.37489/2588-0527-2022-1-63-73
Введение / Introduction
В мире на рак молочной железы (РМЖ) приходится около 30 % случаев всех видов онкопатологии у женщин, а соотношение смертности к заболеваемости составляет 15 % [1]. Около 60–75 % вновь диагностированных случаев рака молочной железы являются положительными по рецепторам эстрогена (ER), в этих случаях назначается эндокринная терапия, например тамоксифеном или ингибиторами ароматазы [2]. Эндокринная терапия в течение 5–10 лет является стандартным методом лечения женщин с ER-положительным раком молочной железы [3].
Тамоксифен (ТАМ) — ключевой элемент эндокринной терапии, назначаемой больным РМЖ, относится к препаратам с очень сложным метаболизмом. Тамоксифен метаболизируется различными ферментами цитохрома Р450 в его первичные метаболиты, такие как N-десметил-тамоксифен (NDM-тамоксифен) и 4-гидрокси-тамоксифен, после чего происходит второе превращение его первичных метаболитов в активный метаболит эндоксифен [4].
Несмотря на проводимую эндокринную терапию, примерно у 30 % пациентов с раком молочной железы наблюдается рецидив заболевания в течение 15 лет после лечения, что указывает на широкую вариабельность клинического ответа на лечение тамоксифеном, на которую влияют как негенетические (возраст, пол), так и генетические факторы.
Среди генетических факторов наиболее изученным фактором была вариация гена CYP2D6, кодирующего соответствующий метаболический фермент печени. Хотя он присутствует почти во всех метаболических превращениях тамоксифена, однако CYP2D6 является единственным ферментом, который превращает NDM-тамоксифен в эндоксифен, поэтому CYP2D6 считается критическим ферментом метаболизма ТАМ [5]. «CYP2D6/Тамоксифен» был признан второй по важности парой «ген / тип препарата» согласно опросу, проведённому членами Американского общества клинической фармакологии и терапии в 2010 г., что указывает на важность генотипа CYP2D6 в опосредовании терапевтических эффектов тамоксифена [6].
Во многих исследованиях были проанализированы клинические последствия носительства генотипа CYP2D6 и его взаимосвязь с эффективностью ТАМ, описана важность генотипирования по CYP2D6 из-за худшего клинического исхода среди пациентов с отсутствием или пониженной ферментативной активностью фермента CYP2D6, однако другие авторы не смогли найти подобную связь [7–10].
Следует отметить, что существует множество исследований, демонстрирующих связь между генотипом CYP2D6 и исходом лечения ТАМ, хотя CYP2C9, CYP3A и другие ферменты также вносят вклад в его метаболизм [11].
Таким образом, фармакогеномика может сыграть важную роль в оптимизации адъювантной терапии тамоксифеном. Также имеются сообщения о повышенном коэффициенте риска для женщин с уменьшенными функциональными аллелями, и этот эффект возрос после поправки на соблюдение режима терапии тамоксифеном [12]. Различия в генах, кодирующих фермент CYP2D6 и другие ферменты, также могут быть основными факторами предрасположенности к возникновению нежелательных лекарственных реакций (НЛР) при приёме ТАМ [13], что в свою очередь приведёт к снижению приверженности пациенток к терапии и, как следствие, к снижению выживаемости.
Цель и методы исследования / Purpose and methods of research
В данной статье представлены результаты проспективного исследования «Популяционное исследование клинического значения генетического полиморфизма ферментов метаболизма и транспортёров тамоксифена при раке молочной железы» у пациенток c РМЖ, радикально пролеченных и получавших эндокринотерапию ТАМ в адъювантном режиме амбулаторно в период 2018–2019 гг., выполненного в ФГБОУ ДПО РМАНПО Минздрава России в рамках госзадания ЕГИСУ НИОКТР № 121110800062-6 «Новые фармакогенетические биомаркеры безопасности фармакотерапии некоторых социально значимых заболеваний».
Целью исследования был анализ нежелательных лекарственных реакций тамоксифена, применяемого в адъювантном режиме у пациенток с раком молочной железы, во взаимосвязи с носительством генетических полиморфизмов генов, кодирующих ферменты цитохромной системы Р450 и белки-транспортёры лекарственных средств.
Материалы и методы / Materials and methods
120 женщин с люминальным РМЖ I–III стадий, принимающие ТАМ в адъювантном режиме, были исследованы на наличие полиморфизмов генов CYP2D6, CYP2C, CYP3A: CYP2D6*4, CYP3A5*3, CYP2C9*2, CYP2C9*3, CYP2C19*2, CYP2C19*3, а также полиморфного маркера гена ABCB1 (С3435Т), кодирующего транспортный белок гликопротеина-Р. Аллельные варианты определялись с помощью метода полимеразной цепной реакции в режиме реального времени в Научно-исследовательском институте молекулярной и персонализированной медицины ФГБОУ ДПО РМАНПО Минздрава России (дир-р — д. м. н. Мирзаев К.Б.). Материал исследования — буккальный эпителий (двукратный забор). Всеми участницами исследования перед взятием материала было подписано информированное добровольное согласие. В качестве источников медицинской информации использовались данные анамнеза и выписки из историй болезни, на основании которых заполнялись специально созданные нами анкеты. Исследование одобрено комитетом по этике научных исследований ФГБОУ ДПО РМАНПО Минздрава России.
Статистическая обработка результатов. При статистической обработке результатов использовали программу SPSS Statistics 26.0 (США). Проверка нормальности распределения проводилась методом Колмогорова — Смирнова с поправкой Лиллиефорса. При нормальном распределении данных количественный показатель представлялся в виде средней арифметический (М), с стандартным отклонением (±SD) и 95 % доверительным интервалом (95 % ДИ). В случае ненормального распределения данных количественный показатель представлялся в виде медианы (Ме) с интерквартильным размахом (25–75 %Q). Межгрупповые различия оценивались при помощи t-критерия Стьюдента при нормальном распределении, а также с помощью U-критерия Манна — Уитни при ненормальном распределении. Сравнительный анализ независимых категориальных переменных использовался с применением χ2 Пирсона либо точного теста Фишера, а также с использованием post-hoc анализа. Номинальный показатель представлялся абсолютным числом наблюдений, приведена процентная доля признака в подгруппах. Для построения предсказательных моделей использовали метод бинарной логистической регрессии с указанием грубого отношения шансов (COR) и скорректированного отношения шансов (AOR). Был применён ROC-анализ для коррекции точки отсечения предсказательной функции P. Все статистические тесты проводились при 95 % уровне значимости (пороговое значение p для подтверждения статистической значимости — менее 0,05). Статистическая мощность >80 %.
Результаты и их обсуждение / Results and their discussion
Описание клинической группы представлено в таблице 1.
Таблица 1
Обобщённые демографические, клинические: гинекологический статус, статус эндометрия, мутационный статус, статус
опухоли, методы проведённого лечения, исходы заболевания —
и анамнестические (приём ТАМ и НЛР на терапии ТАМ)
данные исследуемой группы пациентов (n = 120)
Table 1
Generalized demographic, clinical: gynecological status, endometrial
status, mutational status, tumor status, methods of treatment, disease
outcomes, and anamnestic (admission ТАМ and ADR on therapy
ТАМ) data of the study group of patients (n = 120)

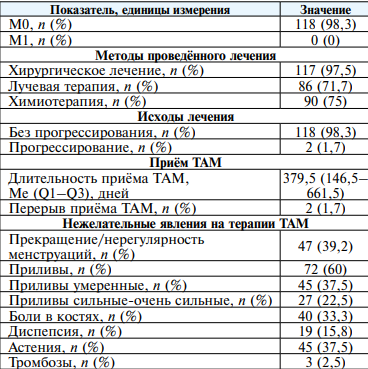
Результаты генетического тестирования представлены в таблице 2.
Таблица 2
Изначальные генетические данные исследуемой группы пациентов
Table 2
Initial genetic data of the studied group of patients
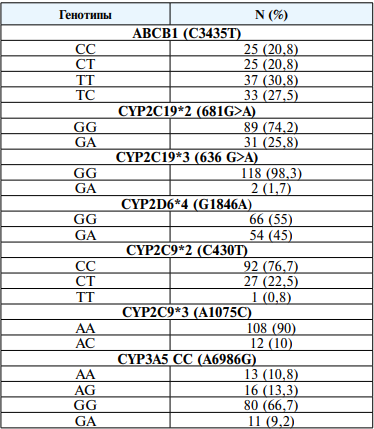
Анализ полученных результатов проводился в два этапа. На первом этапе проведена сравнительная оценка в подгруппах по наличию или отсутствиюнежелательных лекарственных реакций (НЛР) на фоне эндокринной терапии тамоксифеном (ТАМ) у пациенток с РМЖ. На втором этапе разрабатывались прогностические модели развития НЛР при эндокринотерапии ТАМ.
Результаты первого этапа показали, что в подгруппе пациенток с приливами чаще выявляли больший размер опухоли при анализе T (p = 0,048), реже встречали TC аллель ABCB1 (C3435T) (p < 0,001), GA аллель CYP2D6*4 (G1846A) (p < 0,001) и аллель GG гена CYP3A5 CC (A6986G) (p = 0,048), однако у них чаще обнаруживался GG аллель CYP2D6*4 (G1846A) (p < 0,001). При этом эти пациентки больше набирали вес (p = 0,05), у них чаще встречалась гиперплазия эндометрия (p = 0,037) и реже лучевая терапия в анамнезе (p = 0,021).
Подгруппа пациенток с болями в костях была старше по возрасту (p = 0,021), c меньшим размером опухоли при анализе T3 (р = 0,03). У них чаще встречался аллель CT и реже аллель TC гена ABCB1 (C3435T) (p = 0,033 и p = 0,009 соответственно), чаще обнаруживался GG аллель CYP2D6*4 (G1846A) (p = 0,002) и АА аллель CYP2C9*3 (А1075С) (p = 0,008) и аллель AA и AG (p = 0,031 и p = 0,048 соответственно), но реже — GG аллель CYP3A5 CC (A6986G) (p = 0,02). При этом в данной подгруппе отмечалась тенденция к более высокому ИМТ (p = 0,056), эти пациентки чаще и больше набирали вес (p = 0,007 и p = 0,028 соответственно), с большим количеством беременностей (p = 0,032) и абортов (p = 0,026) в анамнезе, и у них чаще отмечалась менопауза (p = 0,038). Следует отметить, пациентки с болями в костях чаще страдали приливами (p = 0,018), диспепсией (p < 0,001) и астенией (p < 0,001), но имели более низкие значения Ki 67 (p = 0,02).
В подгруппе пациенток с диспепсией значимо чаще встречался TT аллель ABCB1 (C3435T) (p = = 0,013), реже ТС аллель ABCB1 (C3435T) (p = 0,023), GG аллель CYP2D6_4 (G1846A) (p = 0,006), значимо больше набирали вес (p = 0,001), значимо чаще страдали от сильных или очень сильных приливов (p = 0,036) чаще страдали от болей в костях (p = 0,001), но со значимо меньшими значениями Ki 67 (p = 0,033).
В подгруппе пациенток с гиперплазией эндометрия (ГЭ) была больше выражена распространённость онкологического процесса при анализе N3 (p = 0,008), значимо чаще встречался TT аллель ABCB1 (C3435T) (p = 0,028), эти пациентки чаще рожали (p = 0,019), страдали от приливов (79,2 и 55,2 %, p = 0,037) и аномальных маточных кровотечений (АМК) (52,4 и 2,1 % соответственно, p = 0,011), а также от астении (62,5 и 31,3 % соответственно, p = 0,008), чем подгруппа пациентов без гиперплазии эндометрия.
Подгруппа пациенток с АМК чаще характеризовалась более развитым онкологическим процессом при анализе значений T (p = 0,023) и N3 (p = 0,031), кроме того в ней чаще выявлялась гиперплазия эндометрия (86,7 и 10,5 % соответственно, p < 0,001), они чаще страдали от сильных / очень сильных приливов (53,3 и 18,1 % соответственно, p = 0,005) и астении (66,7 и 33,3 % соответственно, p = 0,021), чем пациенты без АМК.
В подгруппе пациенток с астенией был меньше распространён метастатический процесс при анализе встречаемости стадии N0 (p = 0,018) и N1 (p = 0,044), реже встречался аллель CC CYP2C9*2 (С430Т), но чаще — AA аллель CYP2C9*3 (А1075С) (p = 0,03). Кроме того, в данной подгруппе отмечено меньше количество выкидышей в анамнезе (p = 0,019), но чаще — гиперплазия эндометрия (p = 0,008) и АМК (p = 0,021), при этом они чаще страдали от сильных / очень сильных приливов (p = 0,028) и болей в костях (p < 0,001). Важным фактом явилось обнаружение тенденции к более частому возникновению тромбозов в подгруппе пациенток с астенией (p = 0,051).
Подгруппа пациентов с полипом эндометрия (ПЭ) по возрасту была моложе (p = 0,035), при этом имела большее снижение массы тела при приёме тамоксифена (p < 0,001), чем подгруппа без ПЭ.
Полученные нами данные, что выявление TC аллеля гена ABCB1 (C3435T) ассоциируется со снижением вероятности развития приливов и болей в костях при приёме ТАМ (p = 0,001 и 0,009 соответственно), в то время как TT аллель ассоциируется с повышенным риском развития диспепсии (p = 0,013), подтверждаются ранее проведёнными исследованиями. По данным литературы, пациентам с гетерозиготным генотипом ABCB1 необходимо более тщательное динамическое наблюдение. Так, в исследовании Sensorn I c соавт. 2016 г. было продемонстрировано, что эта группа пациентов имеет более высокий риск рецидива РМЖ в течение жизни за счёт того, что полиморфизмы ABCC2 и ABCB1 независимо связаны с костным метастазированием [17].
Выявленный нами факт, что аллель GG гена CYP2D6*4 (G1846A), характерный для фенотипа «быстрых метаболизаторов», ассоциируется с риском развития приливов (р < 0,001), болей в костях (p = 0,002), диспепсии (p = 0,006) при приёме тамоксифена, в то время как наличие GA аллеля того же гена, характерного для фенотипа «промежуточного метаболизатора», снижает вероятность развития приливов (р < 0,001), болей в костях (p = 0,002), диспепсии (p = 0,006), также находит подтверждение в научной литературе. Полученные нами данные согласуются с результатами работы Irvin WJr с соавт., продемонстрировавшей более высокие уровни концентрации эндоксифена в начале исследования в группе быстрых метаболизаторов, чем в группах промежуточных и медленных метаболизаторов (p < 0,001) [18]. Исследование Schroth W с соавт. также показало значительно более высокий риск рецидивирования у гетерозиготных экстенсивных и промежуточных метаболизаторов, а также у медленных метаболизаторов по сравнению с гомозиготными экстенсивными метаболизаторами [19]. Однако многие крупные исследования не подтвердили эту взаимосвязь, в связи с чем разногласия в рекомендациях по практическому применению генетического исследования полиморфизмов CYP2D6, в качестве решающего инструмента при определении оптимальной стратегии адъювантной эндокринотерапии, сохраняются и по сегодняшний день. Так, Голландская группа рекомендует рассмотреть вопрос о замене ТАМ препаратом из группы ингибиторов ароматазы и/или избегать одновременного использования ингибиторов фермента CYP2D6 из-за повышенного риска рецидива РМЖ в группе медленных и промежуточных метаболизаторов [20].
Полученные нами результаты, касающиеся обнаружения СT аллеля гена CYP2C9*2 (С430Т) со значимыми ассоциациями с развитием диспепсии (p = 0,013), в то время как выявление СС аллеля снижает риск развития диспепсии (p = 0,015), а также обнаружение AA аллеля гена CYP2C9*3 (А1075С) со значимыми ассоциациями с повышенным риском развития болей в костях (p = 0,008), астении (p = 0,03), в то же время выявление AC аллеля CYP2C9*3 (А1075С) снижает вероятность развития болей в костях (p = 0,008) или астении (p = 0,03) при приёме ТАМ, — согласуются с литературными данными. Так, у носителей аллелей CYP2C9*2 и/или CYP2C9*3 по сравнению с гомозиготными носителями дикого типа гена было обнаружено статистически значимое снижение концентрации активных метаболитов ТАМ [21].
Обнаруженными нами данные о том, что GG аллель гена CYP3A5 CC (A6986G) ассоциируется со снижением риска развития болей в костях при приёме тамоксифена (p = 0,02), но реже встречается у пациенток с приливами (р < 0,001), а АА или GA аллели CYP3A5 CC (A6986G) статистически более значимо повышают риск развития диспепсии, чем при носительстве GG аллеля (p = 0,06; p = 0,15 и р < 0,001 соответственно), согласуются с данными других исследований, по результатам которых также наблюдалось некоторое снижение концентрации эндоксифена в плазме у гомозигот по CYP3A5*3 относительно пациентов, имеющих хотя бы одну активную аллель CYP3A5*1 [22][23].
Результатом второго этапа / The result of the second stage явилось построение 4 логистических функций, позволивших разработать прогностические модели для определения таких нежелательных лекарственных реакций у пациенток с РМЖ, находящихся на эндокринотерапии ТАМ, как приливы, диспепсия, боли в костях и астения.
1. Была разработана прогностическая модель для определения вероятности возникновения приливов при приёме тамоксифена в зависимости от анамнестических и генетических факторов риска с помощью метода бинарной логистической регрессии. В результате пошагового отбора факторов методом исключения была получена логистическая функция (1), включающая 7 предикторов:
Наблюдаемая зависимость описывается уравнением:
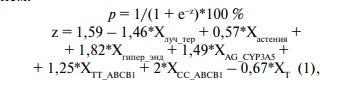
где p — вероятность развития приливов (в долях единицы);
Xлуч_тер — лучевая терапия (0 — нет, 1 — есть);
Xастения — астения (0 — нет, 1 — есть);
Xгипер_энд — гиперплазия эндометрия (0 — нет, 1 — есть);
XAG_CYP3A5 — AG аллель CYP3A5 (0 — нет, 1 — есть);
XTT_ABCB1 — TT аллель ABCB1 (0 — нет, 1 — есть);
XCC_ABCB1 — CC аллель ABCB1 (0 — нет, 1 — есть);
XT — распространённость первичной опухоли (T) по классификации TNM.
Исходя из значений регрессионных коэффициентов, такие факторы, как астения, гиперплазия эндометрия, AG аллель CYP3A5, TT аллель ABCB1 и СС аллель ABCB1, имеют прямую связь с вероятностью возникновения приливов. В то время как наличие в анамнезе лучевой терапии и более развитое распространение опухоли (T) по классификации TNM имеют обратную связь с возникновением приливов.
Полученная регрессионная модель была статистически значимой (p < 0,001). Исходя из значения коэффициента детерминации Найдлжеркерка, модель (1) учитывает 32,9 % факторов, определяющих развитие приливов.
В таблице 3 определены параметры связи каждого из предикторов модели с шансами выявления приливов.
Таблица 3
Оценка связи предикторов модели (1) с шансами выявления приливов
Table 3
Evaluation of the relationship of predictors of the model (1) with the chances of detecting tides
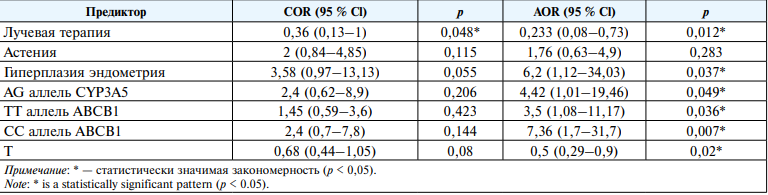
С помощью ROC-анализа было определено наиболее оптимальное значение прогностической функции p. Полученная кривая представлена на рисунке 1.
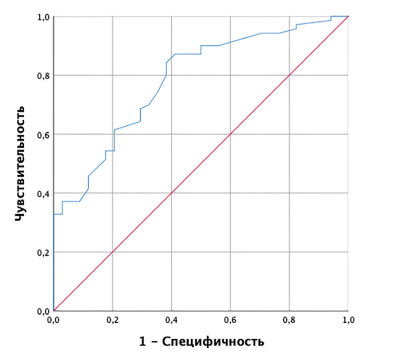
Рис. 1. ROC-кривая, характеризующая зависимость
прогноза приливов при приёме ТАМ от значения логистической функции p
Fig. 1. The ROC curve characterizing the dependence of
the forecast of tides at reception ТАМ on the value of the
logistic function p
Площадь под ROC-кривой составила 0,783±0,046 (95 % ДИ: 0,692–0,874). Значение логистической функции p в точке сut-off составило 0,607. Пациентам со значениями p, равными 0,607 или выше, предсказывался высокий риск развития приливов. При p < 0,607 прогнозировался низкий риск развития приливов. Чувствительность модели (1) при выбранном значении точки cut-off составила 82,9 % (58 верных прогнозов из 70 случаев наличия приливов), специфичность составила 61,8 % (21 верный прогноз из 34 случаев отсутствия приливов). Общая диагностическая эффективность — 76 %.
2. Была разработана прогностическая модель для определения вероятности возникновения диспепсии при приёме тамоксифена в зависимости от анамнестических и генетических факторов риска с помощью метода бинарной логистической регрессии. В результате пошагового отбора факторов методом исключения была получена логистическая функция (2), включающая 9 предикторов:
Наблюдаемая зависимость описывается уравнением:
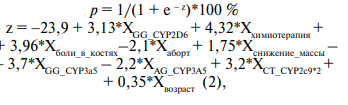
где p — вероятность развития диспепсии (в долях единицы);
XGG_CYP2D6 — GG — аллель CYP2D6 (0 — нет, 1 — есть);
Xхимиотерапия — химиотерапия в анамнезе (0 — нет, 1 — есть);
Xболи_в_костях — наличие болей в костях (0 — нет, 1 — есть);
Xаборт — количество абортов в анамнезе;
Xснижение_массы — снижение массы тела (кг); XGG_CYP3A5 — GG аллель CYP3A5 (0 — нет, 1 — есть);
XAG_CYP3A5 — AG аллель CYP3A5 (0 — нет, 1 — есть);
XCT_CYP2C9*2 — CT аллель CYP2C9*2 (0 — нет, 1 — есть);
Xвозраст — возраст (лет).
Исходя из значений регрессионных коэффициентов, такие факторы, как GG аллель CYP2D6, химиотерапия в анамнезе, боли в костях, снижение массы тела, CT аллель CYP2C9*2 и возраст, имеют прямую связь с вероятностью возникновения диспепсии. В то время как количество абортов в анамнезе, GG аллель CYP3A5 и AG аллель CYP3A5 имеют обратную связь с возникновением диспепсии.
Полученная регрессионная модель была статистически значимой (p < 0,001). Исходя из значения коэффициента детерминации Найдлжеркерка, модель (1) учитывает 66,1 % факторов, определяющих развитие диспепсии.
Чувствительность модели (2) составила 64,7 % (11 верных прогнозов из 17 случаев диспепсии), специфичность составила 96,6 % (84 верных прогноза из 87 случаев отсутствия диспепсии). Диагностическая эффективность модели составила 91,3 %.
В таблице 4 определены параметры связи каждого из предикторов модели с шансами выявления диспепсии.
Таблица 4
Оценка связи предикторов модели (2) с шансами выявления диспепсии
Table 4
Evaluation of the relationship of predictors of model (2) with the chances of detecting dyspepsia
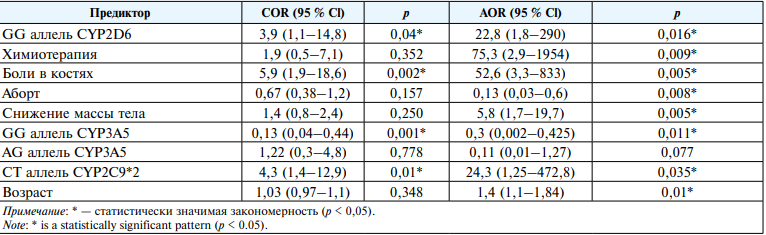
3. Была разработана прогностическая модель для определения вероятности возникновения болей в костях при приёме тамоксифена в зависимости от анамнестических и генетических факторов риска с помощью метода бинарной логистической регрессии. В результате пошагового отбора факторов методом исключения была получена логистическая функция (3), включающая 8 предикторов:
Наблюдаемая зависимость описывается уравнением:
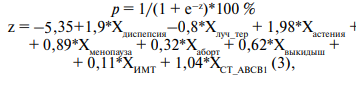
где p — вероятность развития болей в костях (в долях единицы);
Xдиспепсия — наличие диспепсии (0 — нет, 1 — есть);
Xлуч_тер — лучевая терапия в анамнезе (0 — нет, 1 — есть);
Xастения — наличие астении (0 — нет, 1— есть);
Xменопауза — наличие менопаузы (0 — нет, 1— есть);
Xаборт — количество абортов в анамнезе;
Xвыкидыш — количество выкидышей в анамнезе;
XИМТ — индекс массы тела (кг/м2 );
XCT_ABCB1 — CT аллель ABCB1 (0 — нет, 1 — есть).
Исходя из значений регрессионных коэффициентов, такие факторы, как диспепсия, астения, менопауза, количество абортов и выкидышей в анамнезе, а также повышение ИМТ и CT аллель ABCB1, имеют прямую связь с вероятностью возникновения болей в костях. В то время как лучевая терапии в анамнезе имеет обратную связь с возникновением болей в костях.
Полученная регрессионная модель была статистически значимой (p < 0,001). Исходя из значения коэффициента детерминации Найдлжеркерка, модель (1) учитывает 46,2 % факторов, определяющих развитие диспепсии.
Чувствительность модели (3) составила 64,9 % (24 верных прогноза из 37 случаев болей в костях), специфичность составила 85,1 % (57 верных прогнозов из 67 случаев отсутствия болей в костях). Диагностическая эффективность модели составила 78 %.
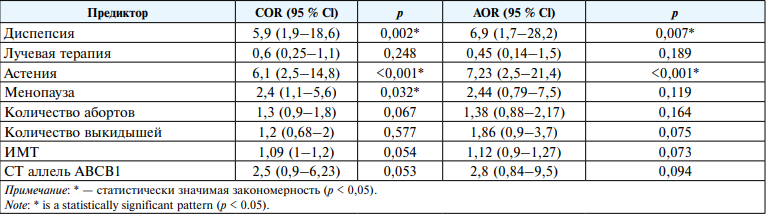
В таблице 5 определены параметры связи каждого из предикторов модели с шансами выявления болей в костях.
Таблица 5
Оценка связи предикторов модели (3) с шансами выявления болей в костях
Table 5
Evaluation of the relationship of predictors of the model (3) with the chances of detecting bone pain
4. При разработке прогностической модели для определения вероятности возникновения астении при приёме тамоксифена в зависимости от анамнестических и генетических факторов риска с помощью метода бинарной логистической регрессии использовались данные 103 пациенток. В результате пошагового отбора факторов методом исключения была получена логистическая функция (4), включающая 7 предикторов:
Наблюдаемая зависимость описывается уравнением:
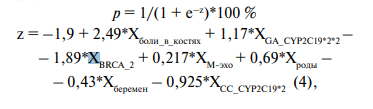
где p — вероятность развития астении (в долях единицы);
Xболи_в_костях — боли в костях (0 — нет, 1 — есть);
XGA_CYP2C19*2*2 — GA аллель CYP2C19*2*2 (0 — нет, 1 — есть);
XBRCA_2 — наличие гена BRCA 2 (0 — нет, 1 — есть);
XМ-эхо — М-эхо (мм); Xроды — количество родов в анамнезе;
Xберемен — количество беременностей в анамнезе;
XCC_CYP2C19*2 — CC генотип CC_CYP2C19*2 (0 — нет, 1 — есть).
Исходя из значений регрессионных коэффициентов, такие факторы, как боли в костях, GA аллель CYP2C19*2*2, М-эхо, количество родов в анамнезе, имеют прямую связь с вероятностью возникновения астении. В то время как наличие BRCA 2, количество беременностей в анамнезе и СС аллель CYP2C19*2 имеют обратную связь с возникновением астении.
Полученная регрессионная модель была статистически значимой (p < 0,001). Исходя из значения коэффициента детерминации Найдлжеркерка, модель (1) учитывает 43,9 % факторов, определяющих развитие диспепсии.
Чувствительность модели (4) составила 65,9 % (27 верных прогнозов из 41 случая астении), специфичность составила 88,7 % (55 верных прогнозов из 62 случаев отсутствия астении). Диагностическая эффективность модели составила 79,6 %.
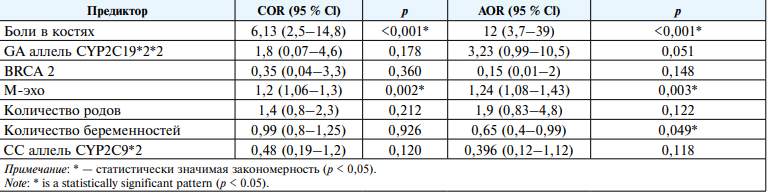
В таблице 6 определены параметры связи каждого из предикторов модели с шансами выявления астении.
Таблица 6
Оценка связи предикторов модели (4) с шансами выявления астении
Таблица 6
Evaluation of the relationship of predictors of the model (4) with the chances of detecting asthenia
Заключение / Conclusion
Таким образом, фармакогеномика играет важную роль в развитии адъювантной терапии для профилактики рецидивов РМЖ. Но несмотря на доступность большого количества информации о взаимосвязи между полиморфизмами гена, кодирующего фермент CYP2D6, и лечением РМЖ тамоксифеном, а также тот факт, что Управление по контролю за качеством пищевых продуктов и медикаментов (FDA) ранее установило изменение в инструкции к препарату согласно данной информации, не было никаких конкретных рекомендаций, установленных для клиницистов в клинической практике. Это связано с наличием многочисленных противоречий в результатах текущих исследований, проанализированных международным консорциумом по фармакогеномике тамоксифена и другими группами [24].
По результатам проведённого ассоциативного анализа гипотеза о роли генетических полиморфизмов системы цитохромов CYP и транспортёров Рg ТАМ в развитии побочных эффектов эндокринотерапии РМЖ подтвердилась частично. Достоверные связи были получены не для всех изучаемых нежелательных лекарственных реакций (НЛР), а только для приливов, болей в костях, диспепсии и астении, свидетельствующие о клинической значимости различных генетических полиморфизмов CYP2D6, CYP3A5, CYP2C9 и ABCB1, в большей степени отвечающих за повышенные уровни концентрации ТАМ и его метаболитов в плазме.
Наличие ярко выраженных НЛР свидетельствует о высокой концентрации активных метаболитов и эффективности терапии ТАМ, однако может препятствовать достаточной приверженности пациенток к проводимой терапии. Однако полное отсутствие НЛР может косвенно свидетельствовать о недостаточной фармакологической активности препарата из-за наличия одной или нескольких клинически значимых мутаций в генах системы цитохрома Р450 и Р-гликопротеина.
Проведённый комплексный ассоциативный анализ позволил нам с использованием математического моделирования построить прогностические модели риска развития таких НЛР при приёме ТАМ, как приливы, диспепсия, боли в костях и астения. Данные прогностические модели продемонстрировали высокую диагностическую эффективность, что позволяет имплементировать их в клиническую практику. Таким образом, модели, включающие как генетические, так и негенетические детерминанты, могут способствовать дальнейшему улучшению предсказания индивидуального ответа на тамоксифен у пациенток с РМЖ [4].
Кроме того, необходимо разработать специальные клинические рекомендации по проведению фармакогеномного тестирования, что помогло бы расширить наши знания для разработки более эффективных и оптимальных методов противорецидивного лечения выживших после рака молочной железы [25].
Этика. Исследование одобрено комитетом по этике научных исследований ФГБОУ ДПО РМАНПО Минздрава России, протокол № 1 от 17 января 2017 года.
Список литературы
1. Siegel RL, Miller KD, Jemal A. Cancer statistics, 2020. CA Cancer J Clin. 2020;0:1–24.
2. Huang B, Warner M, Gustafsson JA. Estrogen receptors in breast carcinogenesis and endocrine therapy. Mol Cell Endocrinol. 2015;418(Pt 3): 240–4.
3. Rugo HS, Rumble RB, Macrae E, Barton DL, Connolly HK, Dickler MN, Fallowfield L, Fowble B, Ingle JN, Jahanzeb M, Johnston SR, Korde LA, Khatcheressian JL, Mehta RS, Muss HB, Burstein HJ. Endocrine Therapy for Hormone Receptor-Positive Metastatic Breast Cancer: American Society of Clinical Oncology Guideline. J Clin Oncol. 2016 Sep 1;34(25):3069–3103. DOI: 10.1200/JCO.2016.67.1487
4. Sanchez-Spitman AB, Swen JJ, Dezentje VO, Moes DJAR, Gelderblom H, Guchelaar HJ. Clinical pharmacokinetics and pharmacogenetics of tamoxifen and endoxifen. Expert Rev Clin Pharmacol. 2019 Jun;12(6):523–536. DOI: 10.1080/17512433.2019.1610390
5. Brauch H, Mürdter TE, Eichelbaum M, Schwab M. Pharmacogenomics of tamoxifen therapy. Clin Chem. 2009 Oct;55(10):1770–1782. DOI: 10.1373/clinchem.2008.121756
6. Relling MV, Klein TE. CPIC: Clinical Pharmacogenetics Implementation Consortium of the Pharmacogenomics Research Network. Clin Pharmacol Ther. 2011 Mar;89(3):464–467. DOI: 10.1038/clpt.2010.279
7. Knox SK, Ingle JN, Suman VJ, et al. Cytochrome P450 2D6 status predicts breast cancer relapse in women receiving adjuvant tamoxifen (Tam). J Clin Oncol. 2006;24(18):4S–4S.
8. Saladores P, Mürdter T, Eccles D, Chowbay B, Zgheib NK, Winter S, Ganchev B, Eccles B, Gerty S, Tfayli A, Lim JS, Yap YS, Ng RC, Wong NS, Dent R, Habbal MZ, Schaeffeler E, Eichelbaum M, Schroth W, Schwab M, Brauch H. Tamoxifen metabolism predicts drug concentrations and outcome in premenopausal patients with early breast cancer. Pharmacogenomics J. 2015 Feb;15(1):84–94. DOI: 10.1038/tpj.2014.34
9. Schroth W, Goetz MP, Hamann U, Fasching PA, Schmidt M, Winter S, Fritz P, Simon W, Suman VJ, Ames MM, Safgren SL, Kuffel MJ, Ulmer HU, Boländer J, Strick R, Beckmann MW, Koelbl H, Weinshilboum RM, Ingle JN, Eichelbaum M, Schwab M, Brauch H. Association between CYP2D6 polymorphisms and outcomes among women with early stage breast cancer treated with tamoxifen. JAMA. 2009 Oct 7;302(13):1429–1436. DOI: 10.1001/jama.2009.1420
10. Sanchez-Spitman A, Dezentjé V, Swen J, Moes DJAR, Böhringer S, Batman E, van Druten E, Smorenburg C, van Bochove A, Zeillemaker A, Jongen L, Los M, Neven P, Gelderblom H, Guchelaar HJ. Tamoxifen Pharmacogenetics and Metabolism: Results from the Prospective CYPTAM Study. J Clin Oncol. 2019 Mar 10;37(8):636–646. DOI: 10.1200/JCO.18.00307
11. Binkhorst L, Mathijssen RH, Jager A, van Gelder T. Individualization of tamoxifen therapy: much more than just CYP2D6 genotyping. Cancer Treat Rev. 2015 Mar;41(3):289–299. DOI: 10.1016/j.ctrv.2015.01.002
12. Thompson AM, Johnson A, Quinlan P, Hillman G, Fontecha M, Bray SE, Purdie CA, Jordan LB, Ferraldeschi R, Latif A, Hadfield KD, Clarke RB, Ashcroft L, Evans DG, Howell A, Nikoloff M, Lawrence J, Newman WG. Comprehensive CYP2D6 genotype and adherence affect outcome in breast cancer patients treated with tamoxifen monotherapy. Breast Cancer Res Treat. 2011 Jan;125(1):279–287. DOI: 10.1007/s10549-010-1139-x
13. Joffe H, Deckersbach T, Lin NU, Makris N, Skaar TC, Rauch SL, Dougherty DD, Hall JE. Metabolic activity in the insular cortex and hypothalamus predicts hot flashes: an FDG-PET study. J Clin Endocrinol Metab. 2012 Sep;97(9):3207–3215. DOI: 10.1210/jc.2012-1413
14. Suzanne D Conzen, Lynn Henry N. Managing the side effects of tamoxifen and aromatase inhibitors. Available from: https://www.uptodate.com/contents/managing–the–side–effects–of–tamoxifen–and–aromatase–inhibitors/print?search=tamoxifen.
15. Kedar RP, Bourne TH, Powles TJ, Collins WP, Ashley SE, Cosgrove DO, Campbell S. Effects of tamoxifen on uterus and ovaries of postmenopausal women in a randomised breast cancer prevention trial. Lancet. 1994 May 28;343(8909):1318–1321. DOI: 10.1016/s0140-6736(94)92466-x
16. Goetz MP, Rae JM, Suman VJ, Safgren SL, Ames MM, Visscher DW, Reynolds C, Couch FJ, Lingle WL, Flockhart DA, Desta Z, Perez EA, Ingle JN. Pharmacogenetics of tamoxifen biotransformation is associated with clinical outcomes of efficacy and hot flashes. J Clin Oncol. 2005 Dec 20;23(36):9312– 9318. DOI: 10.1200/JCO.2005.03.3266
17. Sensorn I, Sukasem C, Sirachainan E, Chamnanphon M, Pasomsub E, Trachu N, Supavilai P, Pinthong D, Wongwaisayawan S. ABCB1 and ABCC2 and the risk of distant metastasis in Thai breast cancer patients treated with tamoxifen. Onco Targets Ther. 2016 Apr 12;9:2121–2129. DOI: 10.2147/OTT.S100905
18. Irvin WJ Jr, Walko CM, Weck KE, Ibrahim JG, Chiu WK, Dees EC, Moore SG, Olajide OA, Graham ML, Canale ST, Raab RE, Corso SW, Peppercorn JM, Anderson SM, Friedman KJ, Ogburn ET, Desta Z, Flockhart DA, McLeod HL, Evans JP, Carey LA. Genotype-guided tamoxifen dosing increases active metabolite exposure in women with reduced CYP2D6 metabolism: a multicenter study. J Clin Oncol. 2011 Aug 20;29(24):3232–3239. DOI: 10.1200/JCO.2010.31.4427
19. Schroth W, Goetz MP, Hamann U, Fasching PA, Schmidt M, Winter S, Fritz P, Simon W, Suman VJ, Ames MM, Safgren SL, Kuffel MJ, Ulmer HU, Boländer J, Strick R, Beckmann MW, Koelbl H, Weinshilboum RM, Ingle JN, Eichelbaum M, Schwab M, Brauch H. Association between CYP2D6 polymorphisms and outcomes among women with early stage breast cancer treated with tamoxifen. JAMA. 2009 Oct 7;302(13):1429–1436. DOI: 10.1001/jama.2009.1420
20. Dean L. Tamoxifen therapy and CYP2D6 genotype. Source Medical Genetics Summaries [Internet]. Bethesda (MD): National Center for Biotechnology Information (US); 2012–2014 Oct 7. PMID: 28520357. Available from: https://pubmed.ncbi.nlm.nih.gov/28520357/.
21. Mwinyi J, Vokinger K, Jetter A, Breitenstein U, Hiller C, Kullak- Ublick GA, Trojan A. Impact of variable CYP genotypes on breast cancer relapse in patients undergoing adjuvant tamoxifen therapy. Cancer Chemother Pharmacol. 2014 Jun;73(6):1181–1188. DOI: 10.1007/s00280-014-2453-5
22. Swen JJ, Nijenhuis M, de Boer A, Grandia L, Maitland-van der Zee AH, Mulder H, Rongen GA, van Schaik RH, Schalekamp T, Touw DJ, van der Weide J, Wilffert B, Deneer VH, Guchelaar HJ. Pharmacogenetics: from bench to byte—an update of guidelines. Clin Pharmacol Ther. 2011 May;89(5):662–673. DOI: 10.1038/clpt.2011.34
23. Khan BA, Robinson R, Fohner AE, Muzquiz LI, Schilling BD, Beans JA, Olnes MJ, Trawicki L, Frydenlund H, Laukes C, Beatty P, Phillips B, Nickerson D, Howlett K, Dillard DA, Thornton TA, Thummel KE, Woodahl EL. Cytochrome P450 Genetic Variation Associated with Tamoxifen Biotransformation in American Indian and Alaska Native People. Clin Transl Sci. 2018 May;11(3):312–321. DOI: 10.1111/cts.12542
24. Cronin-Fenton DP, Damkier P. Tamoxifen and CYP2D6: A Controversy in Pharmacogenetics. Adv Pharmacol. 2018;83:65–91. DOI: 10.1016/bs.apha.2018.03.001
25. Chan CWH, Law BMH, So WKW, Chow KM, Waye MMY. Pharmacogenomics of breast cancer: highlighting CYP2D6 and tamoxifen. J Cancer Res Clin Oncol. 2020 Jun;146(6):1395–1404. DOI: 10.1007/s00432-020-03206-w
Об авторах
Е. О. ГолубенкоРоссия
врач акушер-гинеколог
Москва
М. И. Савельева
Россия
д. м. н., профессор кафедры терапии ИНПО им. профессора Е. Н. Дормидонтова
Ярославль
Ж. А. Созаева
Россия
м. н. с. НИИ молекулярной и персонализированной медицины
Москва
А. В. Поддубная
Россия
д. м. н., профессор, академик РАН, зав. каф. онкологии, проректор по учебной работе и международному сотрудничеству
Москва
В. В. Коренная
Россия
к. м. н., доцент кафедры акушерства и гинекологии
Москва
Рецензия
Для цитирования:
Голубенко Е.О., Савельева М.И., Созаева Ж.А., Поддубная А.В., Коренная В.В. Прогностическое моделирование нежелательных лекарственных реакций тамоксифена при раке молочной железы (результаты когортного исследования). Фармакогенетика и фармакогеномика. 2022;(1):63-73. https://doi.org/10.37489/2588-0527-2022-1-63-73
For citation:
Golubenko E.O., Savelyeva M.I., Sozaeva Z.A., Poddubnaya I.V., Korennaya V.V. Predictive modeling of adverse events of tamoxifen therapy for breast cancer (results of a cohort study). Pharmacogenetics and Pharmacogenomics. 2022;(1):63-73. (In Russ.) https://doi.org/10.37489/2588-0527-2022-1-63-73










































